En Nature: “El coronavirus está mutando, ¿importa?”. Las mutaciones del SARS-CoV-2 plantean más preguntas que respuestas.

España es un Estado aconfesional, que no laicista II
08/09/2020
Lo urgente es regular los cuidados paliativos no legislar sobre la eutanasia
11/09/2020Por Ewen Callaway. Publicado en Nature, 585 , 174-177 (2020). 8 de septiembre de 2020. doi: 10.1038 / d41586-020-02544-6. Las diferentes cepas de SARS-CoV-2 aún no han tenido un impacto importante en el curso de la pandemia, pero podrían hacerlo en el futuro.
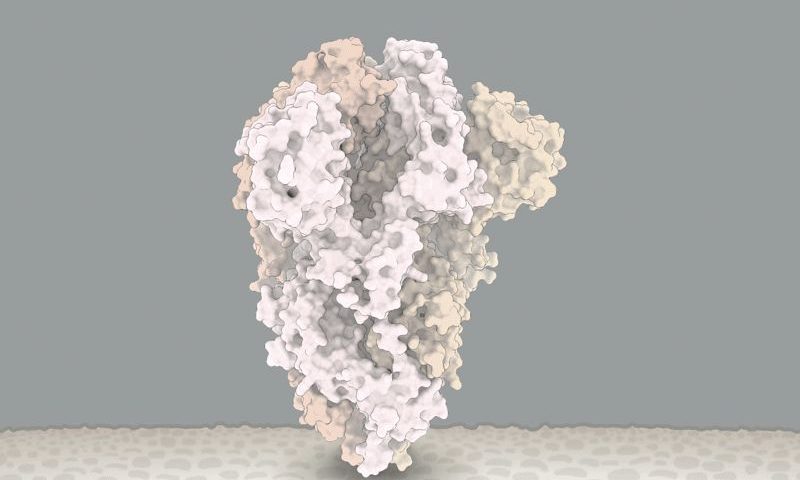
[La imagen de portada: Más detalles en este enlace. Las conformaciones «cerradas» y «abiertas» de la proteína de la espiga en el SARS-CoV-2, que se une a los receptores de las células humanas. Una mutación común (marcada con un círculo) parece hacer que la proteína favorezca las conformaciones abiertas, lo que podría significar que el virus puede ingresar a las células con mayor facilidad. Fuente: datos estructurales de K. Shen y J. Luban]
Cuando COVID-19 se extendió por todo el mundo este año, David Montefiori se preguntó cómo podría estar cambiando el virus mortal detrás de la pandemia a medida que pasa de una persona a otra. Montefiori es un virólogo que ha pasado gran parte de su carrera estudiando cómo las mutaciones casuales del VIH lo ayudan a evadir el sistema inmunológico. Lo mismo podría suceder con el SARS-CoV-2, pensó.
En marzo, Montefiori, quien dirige un laboratorio de investigación de vacunas contra el SIDA en la Universidad de Duke en Durham, Carolina del Norte, se puso en contacto con Bette Korber, experta en la evolución del VIH y colaboradora desde hace mucho tiempo. Korber, un biólogo computacional del Laboratorio Nacional de Los Alamos (LANL) en Sante Fe, Nuevo México, ya había comenzado a rastrear miles de secuencias genéticas de coronavirus en busca de mutaciones que podrían haber cambiado las propiedades del virus a medida que avanzaba por el mundo.
En comparación con el VIH, el SARS-CoV-2 cambia mucho más lentamente a medida que se propaga. Pero una mutación se destacó para Korber. Estaba en el gen que codifica la proteína de la espiga (S), que ayuda a las partículas del virus a penetrar en las células. Korber vio que la mutación aparecía una y otra vez en muestras de personas con COVID-19. En la posición de aminoácido 614 de la proteína de la espiga, el aminoácido aspartato (D, en abreviatura bioquímica) estaba siendo reemplazado regularmente por glicina (G) debido a una falla de copia que alteraba un solo nucleótido en el código de ARN de 29.903 letras del virus. Los virólogos la llamaban mutación D614G.
[Artículo relacionado: ¿A cuántas personas ha matado el coronavirus?]
En abril, Korber, Montefiori y otros advirtieron en una preimpresión publicada en el servidor bioRxiv que “D614G está aumentando en frecuencia a un ritmo alarmante” 1 . Se había convertido rápidamente en el linaje dominante del SARS-CoV-2 en Europa y luego se había afianzado en los Estados Unidos, Canadá y Australia. D614G representaba una “forma más transmisible de SARS-CoV-2”, declaró el documento, una que había surgido como producto de la selección natural.
Estas afirmaciones consternaron a muchos científicos. No estaba claro que el linaje viral D614G fuera más transmisible, o que su aumento indicara algo inusual, dijeron. Pero la alarma se extendió rápidamente por los medios. Aunque muchas noticias incluían advertencias de los investigadores, algunos titulares declararon que el virus estaba mutando para volverse más peligroso. En retrospectiva, Montefiori dice que él y sus colegas lamentan haber descrito el aumento de la variante como «alarmante». La palabra fue eliminada de la versión revisada por pares del artículo, publicada en Cell el 2 de julio .
El trabajo despertó un gran interés en D614G. Incluso aquellos que se mostraron escépticos de que la mutación había cambiado las propiedades del virus estuvieron de acuerdo en que era intrigante, debido a su meteórico ascenso y ubicuidad. Durante meses, ese linaje se ha encontrado en casi todas las muestras secuenciadas de SARS-CoV-2 (consulte ‘Propagación global’). “Esta variante ahora es la pandemia. Como resultado, sus propiedades importan ”, escribieron Nathan Grubaugh, epidemiólogo viral de la Escuela de Salud Pública de Yale en New Haven, Connecticut, y dos colegas en un ensayo de Cell sobre los hallazgos de Korber y Montefiori 3 .
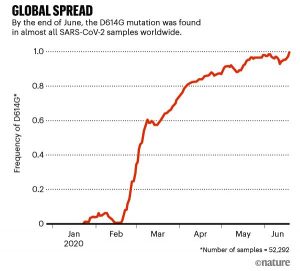
Fuente del gráfico: Ref. 8
Hasta ahora, el resultado de este trabajo es menos claro de lo que sugiere la preimpresión de Montefiori y Korber. Algunos experimentos sugieren que los virus que portan la variante infectan las células con mayor facilidad. Otro trabajo ha revelado posibles buenas noticias: la variante podría significar que las vacunas pueden atacar el SARS-CoV-2 más fácilmente. Pero muchos científicos dicen que no hay pruebas sólidas de que D614G tenga un efecto significativo en la propagación del virus, o que un proceso de selección natural explique su aumento. «El jurado está deliberando», dice Timothy Sheahan, coronavirólogo de la Universidad de Carolina del Norte en Chapel Hill. «Esta mutación puede significar algo, o puede que no».
Los investigadores todavía tienen más preguntas que respuestas sobre las mutaciones del coronavirus, y nadie ha encontrado todavía ningún cambio en el SARS-CoV-2 que deba generar preocupaciones de salud pública, dicen Sheahan, Grubaugh y otros. Pero estudiar las mutaciones en detalle podría ser importante para controlar la pandemia. También podría ayudar a prevenir las mutaciones más preocupantes: aquellas que podrían ayudar al virus a evadir el sistema inmunológico, las vacunas o las terapias con anticuerpos.
Cambio lento
Poco después de que se detectara el SARS-CoV-2 en China, los investigadores comenzaron a analizar muestras virales y a publicar los códigos genéticos en línea. Las mutaciones, la mayoría de ellas alteraciones de una sola base nucleotídica entre virus de diferentes personas, permitieron a los investigadores rastrear la propagación vinculando virus estrechamente relacionados y estimar cuándo el SARS-CoV-2 comenzó a infectar a los humanos.
Los virus que codifican su genoma en ARN, como el SARS-CoV-2, el VIH y la influenza, tienden a detectar mutaciones rápidamente a medida que se copian dentro de sus hospedadores, porque las enzimas que copian el ARN tienden a cometer errores. Después de que el virus del síndrome respiratorio agudo severo (SARS) comenzara a circular en humanos, por ejemplo, desarrolló una especie de mutación llamada deleción (pérdida de bases) que podría haber frenado su propagación 4 .
Pero los datos de secuenciación sugieren que los coronavirus cambian más lentamente que la mayoría de los otros virus de ARN, probablemente debido a una enzima de ‘corrección de pruebas’ que corrige errores de copia potencialmente fatales. Un virus típico del SARS-CoV-2 acumula solo dos mutaciones de una sola letra por mes en su genoma, una tasa de cambio de aproximadamente la mitad que la de la influenza y una cuarta parte de la del VIH, dice Emma Hodcroft, epidemióloga molecular de la Universidad de Basilea. , Suiza.
Otros datos del genoma han enfatizado esta estabilidad: se han secuenciado y hecho públicos más de 90.000 aislamientos (consulte www.gisaid.org ). Dos virus del SARS-CoV-2 recolectados de cualquier parte del mundo difieren en un promedio de solo 10 bases nucleotídicas de su ARN de 29,903, dice Lucy Van Dorp, genetista computacional del University College de Londres, que está rastreando las diferencias en busca de signos de que confieren una ventaja evolutiva.
A pesar de la lenta tasa de mutación del virus, los investigadores han catalogado más de 12.000 mutaciones en los genomas del SARS-CoV-2. Pero los científicos pueden detectar mutaciones más rápido de lo que pueden darles sentido. Muchas mutaciones no tendrán consecuencias en la capacidad del virus para propagarse o causar enfermedades, porque no alteran la forma de ninguna proteína, mientras que aquellas mutaciones que cambian proteínas tienen más probabilidades de dañar el virus que de mejorarlo (ver ‘Catálogo de mutaciones de coronavirus ‘). “Es mucho más fácil romper algo que arreglarlo”, dice Hodcroft, que es parte de Nextstrain , un esfuerzo por analizar los genomas del SARS-CoV-2 en tiempo real.
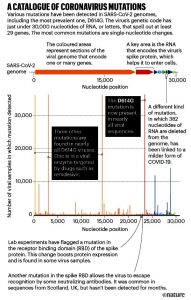
Fuentes: L. Van Dorp et al . ( http://go.nature.com/3GSRNH6 ); Refs 2, 11, 12; BE Young y col. Lancet 396 , 603–611 (2020)
Muchos investigadores sospechan que si una mutación ayudó al virus a propagarse más rápido, probablemente sucedió antes, cuando el virus saltó por primera vez a los humanos o adquirió la capacidad de moverse de manera eficiente de una persona a otra. En un momento en el que casi todos en el planeta son susceptibles, es probable que haya poca presión evolutiva sobre el virus para que se propague mejor, por lo que incluso las mutaciones potencialmente beneficiosas podrían no prosperar. “En lo que respecta al virus, cada persona a la que se le presenta es un buen pedazo de carne”, dice William Hanage, epidemiólogo de la Escuela de Salud Pública TH Chan de Harvard en Boston, Massachusetts. «No hay selección para hacerlo mejor».
¿Difusión más rápida?
Cuando Korber vio la rápida propagación de D614G, pensó que podría haber encontrado un ejemplo de selección natural significativa. La mutación le llamó la atención debido a su posición en la proteína de la espiga, que es un objetivo importante para los anticuerpos ‘neutralizantes’ que se unen al virus y lo vuelven no infeccioso. Y los virus con la mutación también estaban aumentando en frecuencia en más de una parte del mundo.
D614G se detectó por primera vez en virus recolectados en China y Alemania a fines de enero; la mayoría de los científicos sospechan que la mutación surgió en China. Ahora casi siempre está acompañado por tres mutaciones en otras partes del genoma del SARS-CoV-2, posible evidencia de que la mayoría de los virus D614G comparten un ancestro común.
El rápido ascenso de D614G en Europa llamó la atención de Korber. Antes de marzo, cuando gran parte del continente quedó bloqueado, tanto los virus ‘D’ no mutados como los virus ‘G’ mutados estaban presentes, y los virus D prevalecían en la mayoría de los países de Europa occidental que los genetistas muestrearon en ese momento. En marzo, los virus G aumentaron en frecuencia en todo el continente y, en abril, eran dominantes, informaron Korber, Montefiori y su equipo 1 , 2 .
 Imagen: Pasajeros en la estación de tren de Padua en Italia el 12 de marzo, después de que el primer ministro Giuseppe Conte anunciara un posible cierre de los enlaces de transporte para contener el SARS-CoV-2. En ese momento, los virus con la mutación D614G se estaban extendiendo por Europa. Crédito: Roberto Silvino / NurPhoto / Getty
Imagen: Pasajeros en la estación de tren de Padua en Italia el 12 de marzo, después de que el primer ministro Giuseppe Conte anunciara un posible cierre de los enlaces de transporte para contener el SARS-CoV-2. En ese momento, los virus con la mutación D614G se estaban extendiendo por Europa. Crédito: Roberto Silvino / NurPhoto / Getty
Pero la selección natural a favor de los virus G no es la única, ni siquiera la más probable, explicación de este patrón. El dominio europeo de las variantes G podría deberse simplemente al azar, si, por ejemplo, la mutación resultara ser un poco más común en los virus que llegaron a Europa. Un pequeño número de personas parece ser responsable de la mayor parte de la propagación del virus, y una inclinación temprana y casual a favor de los virus G podría explicar la aparente toma de posesión del linaje ahora. Estos «efectos fundadores» son comunes en los virus, especialmente cuando se propagan sin control, como lo hizo el SARS-CoV-2 en gran parte de Europa hasta mediados o finales de marzo.
Korber y sus colegas intentaron descartar un efecto fundador, mostrando en su preprint 1 de abril que el D614G alcanzó el dominio rápidamente en Canadá, Australia y partes de los Estados Unidos (una excepción fue Islandia, donde los virus G presentes al principio de su brote fueron superado por los virus D). Al analizar los datos de hospitalización de Sheffield, Reino Unido, el equipo no encontró evidencia de que los virus portadores de la mutación enfermen más a las personas. Pero los infectados con virus G parecían tener niveles ligeramente más altos de ARN viral en la nariz y la boca que aquellos con virus D.
Muchos científicos no estaban convencidos de que el aumento de D614G fuera notable, o tan relevante para la pandemia. «Pensé que el prepint (anuncio de una publicación antes de su aceptación) era increíblemente prematura», dice Sheahan.
Montefiori dice que su perspectiva y la de Korber sobre D614G fue moldeada por su trabajo sobre el VIH, que ha descubierto que incluso mutaciones aparentemente insignificantes pueden tener un efecto profundo en cómo el sistema inmunológico reconoce ese virus. “Nos alarmó y necesitamos ver si está teniendo un efecto sobre las vacunas”, dice.
Prisa de estudios de laboratorio
Para examinar más a fondo si D614G hizo que el virus fuera más transmisible, Montefiori midió sus efectos en condiciones de laboratorio. No pudo estudiar el virus natural SARS-CoV-2 en su laboratorio, debido a la contención de bioseguridad requerida. Así que estudió una forma genéticamente modificada del VIH que usaba la proteína pico SARS-CoV-2 para infectar células. Estas partículas de ‘pseudovirus’ son un caballo de batalla de los laboratorios de virología: permiten el estudio seguro de patógenos mortales como el virus del Ébola y facilitan la prueba de los efectos de las mutaciones.
 Imagen: El investigador Thomas Nyalile de la Facultad de Medicina de la Universidad de Massachusetts en Worcester prueba el efecto de la variante de proteína de pico D614G sobre la infectividad. El experimento utiliza un pseudovirus que no requiere altos niveles de contención de bioseguridad. Crédito: Jeremy Luban
Imagen: El investigador Thomas Nyalile de la Facultad de Medicina de la Universidad de Massachusetts en Worcester prueba el efecto de la variante de proteína de pico D614G sobre la infectividad. El experimento utiliza un pseudovirus que no requiere altos niveles de contención de bioseguridad. Crédito: Jeremy Luban
El primer equipo en informar sobre experimentos con pseudovirus en D614G, en junio, fue dirigido por Hyeryun Choe y Michael Farzan, virólogos del Instituto de Investigación Scripps en La Jolla, California 5 . Varios otros equipos han publicado estudios similares sobre bioRxiv (los experimentos de Montefiori y los de otro colaborador aparecieron en el artículo 2 de Cell ). Los equipos utilizaron diferentes sistemas de pseudovirus y los probaron en varios tipos de células, pero los experimentos apuntaron a la misma conclusión: los virus que portaban la mutación G infectaban células mucho más hábilmente que los virus D, hasta diez veces más eficientemente, en algunos casos.
En las pruebas de laboratorio, “todos estamos de acuerdo en que D a G hace que las partículas sean más infecciosas”, dice Jeremy Luban, virólogo de la Facultad de Medicina de la Universidad de Massachusetts en Worcester. Pero estos estudios vienen con muchas advertencias, y su relevancia para las infecciones humanas no está clara. “Lo que es irritante es que las personas toman sus resultados en entornos muy controlados y dicen que esto significa algo para la pandemia. Eso, estamos muy lejos de saberlo”, dice Grubaugh. En la mayoría de los casos, los pseudovirus transportan solo la proteína de la espiga del coronavirus, por lo que los experimentos miden solo la capacidad de estas partículas para ingresar a las células, no aspectos de sus efectos dentro de las células, y mucho menos en un organismo. También carecen de las otras tres mutaciones que llevan casi todos los virus D614G. “La conclusión es que no son el virus”, dice Luban.
Algunos laboratorios ahora están trabajando con virus infecciosos del SARS-CoV-2 que difieren solo en un aminoácido. Estos se prueban en cultivos de laboratorio de pulmón humano y células de las vías respiratorias, y en animales de laboratorio como hurones y hámsteres. Para los laboratorios con la experiencia y la capacidad de bioseguridad para manipular virus, “esto es como un trabajo de pan y mantequilla”, dice Sheahan. El primero de esos estudios, dirigido por investigadores de la Rama Médica de la Universidad de Texas en Galveston, se informó en una versión preliminar del 2 de septiembre 6 . Encontró que los virus con la mutación eran más infecciosos que los virus D en una línea celular de pulmón humano y en los tejidos de las vías respiratorias, y que los virus mutados estaban presentes en mayores niveles en las vías respiratorias superiores de los hámsteres infectados 6 .
[Artículo relacionado: Coronavirus reinfections: three questions scientists are asking]
Incluso estos experimentos pueden no ofrecer una claridad absoluta. Algunos estudios muestran que ciertas mutaciones en la proteína de la espiga en el virus del síndrome respiratorio de Oriente Medio (MERS) pueden causar una enfermedad más grave en ratones; sin embargo, otras mutaciones en la proteína muestran muy poco efecto en personas o en camellos, el probable reservorio para humanos. Infecciones por MERS, dice Stanley Perlman, coronavirólogo de la Universidad de Iowa en Iowa City.
La señal más clara de que D614G tiene un efecto sobre la propagación del SARS-CoV-2 en humanos proviene de un ambicioso esfuerzo del Reino Unido llamado COVID-19 Genomics UK Consortium, que ha analizado genomas de alrededor de 25.000 muestras virales. A partir de estos datos, los investigadores han identificado más de 1.300 casos en los que un virus entró en el Reino Unido y se propagó, incluidos ejemplos de virus de tipo D y G.
Un equipo dirigido por Andrew Rambaut, biólogo evolutivo de la Universidad de Edimburgo, Reino Unido, el epidemiólogo Erik Volz, del Imperial College London, y el biólogo Thomas Connor de la Universidad de Cardiff, estudió la propagación en el Reino Unido de 62 cúmulos de COVID-19 sembrados por virus D y 245 por virus G 7 . Los investigadores no encontraron diferencias clínicas en las personas infectadas con cualquiera de los virus. Sin embargo, los virus G tendían a transmitirse un poco más rápido que los linajes que no llevaban el cambio y formaban grupos más grandes de infecciones. Sus estimaciones de la diferencia en las tasas de transmisión rondan el 20%, dice Volz, pero el valor real podría ser un poco más alto o más bajo. «No hay un gran efecto en términos absolutos», dice Rambaut.
Es posible que D614G sea una adaptación que ayude al virus a infectar células o competir con virus que no portan el cambio, mientras que altera poco la forma en que el SARS-CoV-2 se propaga entre las personas a través de una población, dice Rambaut. “Esta podría ser una adaptación genuina a los humanos o algunas células humanas”, coincide Grubaugh, “pero eso no significa que nada cambie. Una adaptación no tiene por qué hacerla más transmisible ”.
Grubaugh cree que D614G ha recibido demasiada atención por parte de los científicos, en parte debido a los artículos de alto perfil que ha obtenido. “Los científicos tienen una loca fascinación por estas mutaciones”, dice. Pero también ve al D614G como una forma de aprender sobre un virus que no tiene mucha diversidad genética. “El virólogo que hay en mí mira estas cosas y dice que sería muy divertido estudiarlas”, dice. «Crea toda esta madriguera de diferentes cosas en las que puedes entrar».
Tendrá compañía. Un estudio intenso de D614G debería ayudar a explicar cómo el SARS-CoV-2 se fusiona con las células, dice Luban, un proceso que podría ser bloqueado por medicamentos o dirigido por una vacuna. En una versión actualizada de sus experimentos con pseudovirus publicados en bioRxiv el 16 de julio 8 , el equipo de Luban utilizó microscopía crioelectrónica para analizar la estructura de las proteínas de la espiga que llevan el cambio D614G. La proteína de la espiga se compone de tres péptidos idénticos en una orientación «abierta» o «cerrada». Investigaciones anteriores han sugerido que al menos dos de los tres péptidos deben estar abiertos para que la partícula viral se fusione con la membrana celular 9, y el equipo de Luban descubrió que los virus que portaban la variante de la espiga G tenían muchas más probabilidades de estar en este estado (ver ‘La mutación que afloja la proteína de la espiga). El trabajo de modelado computacional de Montefiori y Korber, dirigido por Sandrasegaram Gnanakaran, colega de LANL de Korber, llegó a la misma conclusión 10 . “Parece que esta máquina molecular está preparada para funcionar de una manera que D no lo está”, dice Luban.
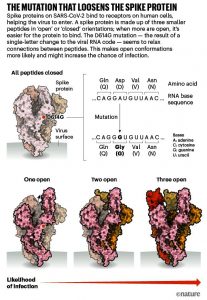 [Imagen: Fuente: datos estructurales de K. Shen y J. Luban]
[Imagen: Fuente: datos estructurales de K. Shen y J. Luban]
No hay escape de los anticuerpos, todavía
La mayoría de la evidencia disponible sugiere que el D614G no impide que los anticuerpos neutralizantes del sistema inmunológico reconozcan el SARS-CoV-2, como le había preocupado Montefiori. Eso podría deberse a que la mutación no se encuentra en el dominio de unión al receptor de la proteína de la espiga (RBD), una región a la que se dirigen muchos anticuerpos neutralizantes: el RBD se une a la proteína receptora celular ACE2, un paso clave en la entrada del virus a las células.
Pero está surgiendo evidencia de que otras mutaciones podrían ayudar al virus a evitar algunos anticuerpos. Un equipo dirigido por los virólogos Theodora Hatziioannou y Paul Bieniasz, de la Universidad Rockefeller en la ciudad de Nueva York, modificó genéticamente el virus de la estomatitis vesicular, un patógeno del ganado, de modo que utilizó la proteína de la espiga del SARS-CoV-2 para infectar células y lo cultivó en la presencia de anticuerpos neutralizantes. Su objetivo era seleccionar mutaciones que permitieran a la proteína de la espiga evadir el reconocimiento de anticuerpos. El experimento generó mutantes de la proteína que eran resistentes a anticuerpos extraídos de la sangre de personas que se habían recuperado del COVID-19, así como a potentes anticuerpos ‘monoclonales’ que se están desarrollando en terapias. Cada una de las mutaciones de la espiga se encontró en secuencias de virus aisladas de pacientes, informa Hatziioannou,11 .
Otros científicos están tratando de adelantarse a la evolución del SARS-CoV-2 al predecir qué mutaciones probablemente sean importantes. Jesse Bloom, virólogo evolutivo del Centro de Investigación del Cáncer Fred Hutchinson en Seattle, Washington, dirigió un equipo que creó casi 4.000 versiones mutadas del RBD de la proteína de la espiga y midió cómo las alteraciones afectaron la expresión de la proteína y su capacidad para unirse a ACE2 (receptor proteico de las células a las que infecta el virus al unirse por la proteína de la espiga). La mayoría de las mutaciones no afectaron ni obstaculizaron estas propiedades, aunque algunas las mejoraron 12 . Algunas de estas mutaciones se han identificado en personas con COVID-19, pero el equipo de Bloom no encontró signos de selección natural para ninguna de las variantes. “Probablemente el virus se une a ACE2 tan bien como lo necesita en este momento”, dice.
[Àrtículo relacionado: Cómo podría desarrollarse la pandemia en 2021 y más allá] – Ver en CiViCa]
Los investigadores no probaron si alguna de las mutaciones permite que el virus frustre la acción de los anticuerpos, pero los resultados de su equipo sugieren que tales cambios son posibles. “Es una posibilidad, pero de ninguna manera una certeza, que el virus adquiera mutaciones que cambien su susceptibilidad a los anticuerpos y la inmunidad”, dice Bloom.
Según la experiencia con otros coronavirus, eso podría llevar años. Los estudios de coronavirus del resfriado común, muestreados en varias estaciones, han identificado algunos signos de evolución en respuesta a la inmunidad. Pero el ritmo del cambio es lento, dice Volker Thiel, virólogo de ARN del Instituto de Virología e Inmunología de Berna. «Estas tensiones se mantienen constantes, más o menos».
Dado que la mayor parte del mundo sigue siendo susceptible al SARS-CoV-2, es poco probable que la inmunidad sea actualmente un factor importante en la evolución del virus. Pero a medida que aumenta la inmunidad en toda la población, ya sea a través de una infección o una vacuna, un goteo constante de mutaciones que evitan el sistema inmunológico podría ayudar al SARS-CoV-2 a establecerse de forma permanente, dice Sheahan, lo que podría causar síntomas en su mayoría leves cuando infecta a personas que tienen algún residuo de inmunidad de una infección o vacunación previa. “No me sorprendería que este virus se mantenga como un coronavirus causante de resfriado más común”. Pero también es posible que nuestras respuestas inmunitarias a las infecciones por coronavirus, incluido el SARS-CoV-2, no sean lo suficientemente fuertes o duraderas como para generar una presión de selección que lleve a cepas de virus significativamente alteradas.
Las mutaciones preocupantes también podrían volverse más comunes si las terapias con anticuerpos no se usan de manera inteligente, si las personas con COVID-19 reciben un anticuerpo, que podría verse frustrado por una sola mutación viral, por ejemplo. Los cócteles de anticuerpos monoclonales, cada uno de los cuales puede reconocer múltiples regiones de la proteína de la espiga, podrían disminuir las probabilidades de que tal mutación se vea favorecida por la selección natural, dicen los investigadores. Las vacunas despiertan menos preocupación en este aspecto porque, al igual que la respuesta inmune natural del cuerpo, tienden a provocar una variedad de anticuerpos.
Incluso es posible que el cambio D614G podría hacer que el virus sea un objetivo más fácil para las vacunas, encontró el equipo de Montefiori en un estudio publicado en bioRxiv el 13 de julio . Ratones, monos y humanos que recibieron una de varias vacunas de ARN experimentales, incluida una que está desarrollando el fabricante de medicamentos Pfizer en la ciudad de Nueva York, produjeron anticuerpos que demostraron ser más potentes para bloquear los virus G que los virus D.
Con los virus G ahora omnipresentes, el hallazgo es «una buena noticia», dice Montefiori. Pero como científico que ha observado la mutación del VIH para eludir muchas vacunas desarrolladas contra él, sigue siendo cauteloso sobre el potencial del SARS-CoV-2 para evadir las respuestas de la humanidad. Luban está de acuerdo: «Debemos mantener los ojos abiertos para cambios adicionales».
Referencias
- Korber, B. y col. Preprint en bioRxiv https://doi.org/10.1101/2020.04.29.069054(2020)
- Korber, B. y col. Cell 182, 812–827 (2020)
- Grubaugh, N., Hanage, W. y Rasmussen, A. Cell 182, 794–795 (2020)
- Muth, D. y col. Sci. Rep. 8, 15177 (2018)
- Zhang, L. y col. Preimpresión en bioRxiv https://doi.org/10.1101/2020.06.12.148726(2020)
- Plante, K. et al. Preprint en bioRxiv https://doi.org/10.1101/2020.09.01.278689(2020)
- Volz, E. M. et al.Preprint at bioRxiv https://doi.org/10.1101/2020.07.31.20166082 (2020)
- Yurkovetskiy, L. et al.Preprint at bioRxiv https://doi.org/10.1101/2020.07.04.187757 (2020)
- Wrapp, D. et al.Science 367, 1260–1263 (2020)
- Mansbach, R. A. et al.Preprint at bioRxiv https://doi.org/10.1101/2020.07.26.219741(2020)
- Weisblum, Y. et al.Preprint at bioRxiv https://doi.org/10.1101/2020.07.21.214759(2020)
- Starr, TN y col. Cell 182, 1295-1310 (2020)
- Weissmann, D. y col. Preprint en bioRxiv