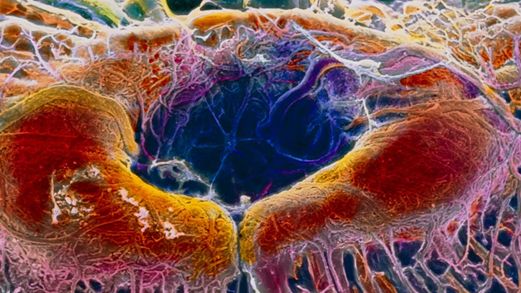
Se aplica una terapia con CRISPR por primera vez directamente en el cuerpo para el tratamiento de una ceguera
Nature.- Seis meses de coronavirus: los misterios que los científicos aún intentan resolver.
29/08/2020
Todo llega cuando tiene que llegar
30/08/2020 Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa. Según publicó Nature 579 , 185 (2020): doi: 10.1038 / d41586-020-00655-8, en su sección de News el pasado 5 de marzo, se ha probado experimentalmente por primera vez una terapia de edición genética con CRISPR-Cas9 para el tratamiento de un trastorno hereditario de ceguera, una afección poco común llamada amaurosis congénita de Leber 10 (LCA10) de la que no se dispone de tratamiento siendo una de las principales causas de ceguera en la infancia. [Imagen de portada: La retina humana: una terapia CRISPR se ha insertado directamente en una persona por primera vez: en el ojo. Prof. P. Motta / Dpto. de Anatomía / Universidad La Sapienza de Roma / SPL].
Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa. Según publicó Nature 579 , 185 (2020): doi: 10.1038 / d41586-020-00655-8, en su sección de News el pasado 5 de marzo, se ha probado experimentalmente por primera vez una terapia de edición genética con CRISPR-Cas9 para el tratamiento de un trastorno hereditario de ceguera, una afección poco común llamada amaurosis congénita de Leber 10 (LCA10) de la que no se dispone de tratamiento siendo una de las principales causas de ceguera en la infancia. [Imagen de portada: La retina humana: una terapia CRISPR se ha insertado directamente en una persona por primera vez: en el ojo. Prof. P. Motta / Dpto. de Anatomía / Universidad La Sapienza de Roma / SPL].
En lugar de hacer el tratamiento con células extraídas del paciente y cultivadas in vitro, que después serían devueltas a la retina, el ensayo se realiza directamente in vivo, inyectando los componentes de la edición génica en las células del ojo, cerca de las células fotorreceptoras.
En el ensayo participa Mark Pennesi, especialista en enfermedades retinianas hereditarias de la Oregon Health & Science University. Pennesi está colaborando con las compañías farmacéuticas Editas Medicine de Cambridge, Massachusetts, y Allergan de Dublín para llevar a cabo el ensayo, que se ha denominado BRILLIANCE.
Si bien es la primera vez que se intenta una edición genómica directamente en el cuerpo, con CRISPR-Cas9, la modificación genética directa en células corporales ya se había intentado anteriormente con otra técnica más compleja y menos precisa que utiliza las nucleasas de dedos de Zinc, por la compañía biotecnológica Sangamo Therapeutics de Brisbane, California. En aquél caso para insertar una copia sana del gen afectado en un lugar determinado del genoma de células hepáticas para una afección metabólica llamada síndrome de Hunter.
En lugar de seguir una terapia convencional de inserción del gen sano en las células, utilizando un vector viral, el tratamiento ensayado por BRILLIANCE con CRISPR-Cas9 trata de editar y así eliminar una mutación en el gen CEP290 causante de LCA10, directamente cerca de las células de la retina. El gen CEP290 es demasiado grande para canalizarlo por virus, por lo que la técnica CRISPR-Cas9 es idónea para modificar solo la parte del gen alterada, en las células de los pacientes con LCA10, con la esperanza de corregir la mutación y reactivar el gen.
Aunque no se han hecho públicos los resultados, la técnica ensayada puede suponer una mejora respecto a otros intentos de corregir este mismo gen.
Si se sabe que es posible mejorar la visión en personas con LCA10, tras aplicar otra terapia mediante un tratamiento experimental llamado sepofarsen asociado con ProQR de Leiden, Países Bajos. Este otro tratamiento utiliza otra técnica de genética molecular llamada terapia antisentido.
La aplicación directa de los componentes de la tecnología CRIPR-Cas9 en las células in vivo, supone un salto significativo en el uso clínico de la edición génica.