Cómo infecta el coronavirus a las células — y por qué Delta es tan peligroso

Creer en lo imposible y aceptar lo inaceptable
29/07/2021
El Comité de Bioética de España se pronuncia sobre aspectos conflictivos relacionados con la regulación del derecho a la objeción de conciencia ante la eutanasia
01/08/2021or Megan Scudellari. Publicado en Nature el 28 de julio de 2021.
Los científicos están despedazando el ciclo vital del SARS-CoV-2 y cómo el virus utiliza trucos para evadir la detección.
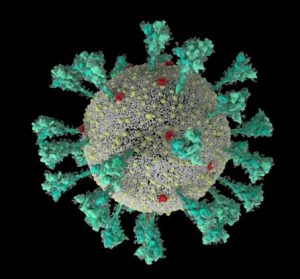 <– A computer simulation of the structure of the coronavirus SARS-CoV-2.Credit: Janet Iwasa, University of Utah
<– A computer simulation of the structure of the coronavirus SARS-CoV-2.Credit: Janet Iwasa, University of Utah
El coronavirus luce un lujoso abrigo de azúcar. «Es sorprendente», pensó Rommie Amaro, mirando la simulación por computadora de una de las proteínas de la espigas de del SARS-CoV-2, que sobresalen de la superficie del virus.
Estaba envuelto en moléculas de azúcar, conocidas como glicanos. «Cuando lo ves con todos los glicanos, es casi irreconocible», dice Amaro, química biofísica computacional de la Universidad de California, San Diego. Muchos virus tienen glicanos que cubren sus proteínas externas, camuflándolos del sistema inmunológico humano como un lobo vestido de oveja. Pero el año pasado, el grupo de laboratorio de Amaro y colaboradores crearon la visualización más detallada hasta ahora de esta capa, basada en datos estructurales y genéticos y representada, átomo por átomo, por una supercomputadora. El 22 de marzo de 2020, publicó la simulación en Twitter. En una hora, un investigador preguntó en un comentario: ¿cuál era el lazo desnudo y sin recubrir que sobresalía de la parte superior de la proteína? Amaro no tenía ni idea. Pero diez minutos más tarde, el biólogo estructural Jason McLellan de la Universidad de Texas en Austin intervino: el bucle no recubierto era un dominio de unión a receptores (RBD), una de las tres secciones de la espiga que se unen a los receptores en las células humanas (Ver A hidden spike).
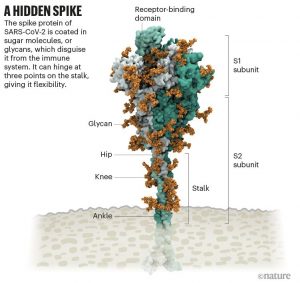
Source: Structural image from Lorenzo Casalino, Univ. California, San Diego (Ref. 1); Graphic: Nik Spencer/Nature –>
[Ver la imagen ampliada en Nature]
En la simulación de Amaro, cuando el RBD sobresale por encima de la nube de glicanos, dos glicanos se abalanzan para bloquearlo en su lugar, como un soporte en una bicicleta. Cuando Amaro mutó los glicanos en el modelo de computadora, el RBD colapsó. El equipo de McLellan construyó una manera de probar el mismo experimento en el laboratorio, y en junio de 2020, los colaboradores habían informado que mutar los dos glicanos reducía la capacidad de la proteína de la espiga para unirse a un receptor de células humanas [1], un papel que nadie ha reconocido previamente en los coronavirus, dice McLellan. Es posible que cortar esos dos azúcares podría reducir la infectividad del virus, dice Amaro, aunque los investigadores aún no tienen una manera de hacerlo.
Desde el inicio de la pandemia de COVID-19, los científicos han estado desarrollando una comprensión detallada de cómo el SARS-CoV-2 infecta las células. Al separar el proceso de infección, esperan encontrar mejores maneras de interrumpirlo a través de mejores tratamientos y vacunas, y aprender por qué las cepas más recientes, como la variante Delta, son más transmisibles.
Lo que ha surgido de 19 meses de trabajo, respaldados por décadas de investigación sobre el coronavirus, es un relato golpe a golpe de cómo el SARS-CoV-2 invade las células humanas (ver ‘Life cycle of the pandemic coronavirus’). Los científicos han descubierto adaptaciones clave que ayudan al virus a agarrarse a las células humanas con una fuerza sorprendente y luego esconderse una vez dentro. Más tarde, a medida que sale de las células, el SARS-CoV-2 ejecuta un paso crucial de procesamiento para preparar sus partículas para infectar aún más células humanas. Estas son algunas de las herramientas que han permitido que el virus se propague tan rápidamente y se cobre millones de vidas. «Por eso es tan difícil de controlar», dice Wendy Barclay, viróloga del Imperial College de Londres.
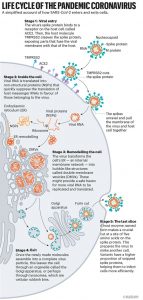 <– Source: Hui (Ann) Liu, Univ. Utah; Graphic: Nik Spencer/Nature
<– Source: Hui (Ann) Liu, Univ. Utah; Graphic: Nik Spencer/Nature
[Ver la imagen ampliada en Nature]
Púas y listo
Comienza con los picos. Cada virión del SARS-CoV-2 (partícula del virus) tiene una superficie externa salpicada de 24-40 proteínas espiga dispuestas al azar que son su clave para fusionarse con las células humanas [2]. Para otros tipos de virus, como la influenza, las proteínas de fusión externas son relativamente rígidas. Los picos de SARS-CoV-2, sin embargo, son tremendamente flexibles y hacen bisagra en tres puntos, según un trabajo publicado en agosto de 2020 por el bioquímico Martin Beck del Instituto Max Planck de Biofísica de Frankfurt, Alemania, y sus colegas [3}. Eso permite que los picos se muevan alrededor, se balanceen y giren, lo que podría facilitarles escanear la superficie de la célula humana y para múltiples picos unirse a una célula. No hay datos experimentales similares para otros coronavirus, pero debido a que las secuencias de proteínas espigas se conservan de manera altamente evolutiva, es justo asumir que el rasgo es compartido, dice Beck.
Cryo-electron tomography images of SARS-CoV-2 virions. Scale bar: 30 nanometres.)Credit: B. Turoňová et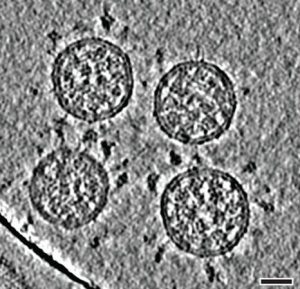 al./Science –>
al./Science –>
Al principio de la pandemia, los investigadores confirmaron que los RBDs de las proteínas espiga del SARS-CoV-2 se unen a una proteína familiar llamada receptor ACE2, que adorna el exterior de la mayoría de las células humanas de la garganta y el pulmón. Este receptor es también el punto de acoplamiento para el SARS-CoV, el virus que causa el síndrome respiratorio agudo severo (SARS). Pero en comparación con el SARS-CoV, el SARS-CoV-2 se une a ACE2 unas 2-4 veces más fuertemente [4], porque varios cambios en el RBD estabilizan sus puntos de enlace al virus [5]. Las variantes preocupantes del SARS-CoV-2 tienden a tener mutaciones en la subunidad S1 de la proteína espiga, que alberga los RBDs y es responsable de la unión al receptor ACE2. (Una segunda subunidad del punto, S2, incita la fusión viral con la membrana de la célula huesped.) La variante Alfa, por ejemplo, incluye diez cambios en la secuencia de la proteína espiga, lo que hace que los RBDs sean más propensos a permanecer en la posición ‘arriba’ [6]. «Esto ayuda al virus a hacer que sea más fácil entrar en las células», dice Priyamvada Acharya, un biólogo estructural del Duke Human Vaccine Institute en Durham, Carolina del Norte, que está estudiando las mutaciones de la espiga.
La variante Delta, que ahora se está extendiendo por todo el mundo, alberga múltiples mutaciones en la subunidad S1, incluyendo tres en la RBD que parecen mejorar la capacidad de la RBD para unirse a ACE2 y evadir el sistema inmune [7].
Entrada restringida
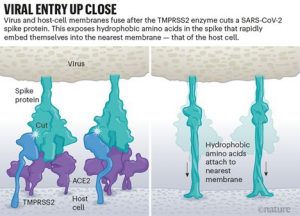
Una vez que los picos virales se unen a la ACE2, otras proteínas de la superficie de la célula huésped inician un proceso que conduce a la fusión de las membranas virales y celulares (ver Viral entry up close).
 <– Source: Janet Iwasa, Univ. Utah; Graphic: Nik Spencer/Nature
<– Source: Janet Iwasa, Univ. Utah; Graphic: Nik Spencer/Nature
El virus que causa el SARS, el SARS-CoV, utiliza cualquiera de las dos enzimas proteasas del huésped para entrar: TMPRSS2 o catepsina L. TMPRSS2 es la ruta más rápida, pero el SARS-CoV a menudo entra en su lugar a través de un endosoma , una burbuja rodeada de lípidos , que se basa en la catepsina L. Sin embargo, cuando los viriones entran en las células por esta vía, las proteínas antivirales pueden atraparlas. El SARS-CoV-2 difiere del SARS-CoV porque utiliza eficientemente TMPRSS2, una enzima que se encuentra en altas cantidades en el exterior de las células respiratorias. En primer lugar, TMPRSS2 corta un sitio en la subunidad S28 del pico. Ese corte expone una serie de aminoácidos hidrofóbicos que se entierran rápidamente en la membrana más cercana: la de la célula huésped. A continuación, la espiga extendida se pliega de nuevo sobre sí misma, como una cremallera, lo que obliga a las membranas virales y celulares a fusionarse.
An animation of the way SARS-CoV-2 fuses with cells.Credit: Janet Iwasa, University of Utah –>
[Ver la imagen animada en Nature]
El virus entonces expulsa su genoma directamente a la célula. Al invadir de esta manera, el SARS-CoV-2 infecta más rápido que el SARS-CoV y evita quedar atrapado en endosomas, según un trabajo publicado en abril por Barclay y sus colegas del Imperial College de Londres [9].
La rápida entrada del virus usando TMPRSS2 explica por qué el medicamento contra la malaria cloroquina no funcionó en los ensayos clínicos como tratamiento de COVID-19, a pesar de los primeros estudios prometedores en el laboratorio [10]. Ésos resultaron haber utilizado las células que dependen exclusivamente de las catepsinas para la entrada endosomal. «Cuando el virus se transmite y se replica en las vías respiratorias humanas, no usa endosomas, por lo que la cloroquina, que es un fármaco disruptor endosomal, no es efectiva en la vida real», dice Barclay.
El descubrimiento también apunta a los inhibidores de la proteasa como una opción terapéutica prometedora para evitar que un virus use TMPRSS2, catepsina L u otras proteasas para entrar en las células huésped. Un inhibidor de TMPRSS2, el mesilato de camostato, aprobado en Japón para tratar la pancreatitis, bloqueó la entrada viral en las células pulmonares [8], pero el fármaco no mejoró los resultados de los pacientes en un ensayo clínico inicial [11].
«Desde mi punto de vista, deberíamos tener inhibidores de la proteasa como antivirales amplios disponibles para combatir nuevos brotes de enfermedades y prevenir futuras pandemias desde el principio», dice Stefan Pöhlmann, director de la Unidad de Biología de Infecciones en el Centro Alemán de Primates en Göttingen, quien ha liderado la investigación sobre la unión a ACE2 y la vía TMPRSS2.
Competición mortal
Los próximos pasos de la infección son más turbios. «Hay muchas más cajas negras una vez que estás dentro de la célula», dice la química Janet Iwasa de la Universidad de Utah en Salt Lake City, quien está desarrollando una animación anotada del ciclo de vida viral. «Hay más incertidumbre e hipótesis que compiten entre sí».
Después de que el virus dispara su genoma de ARN en la célula, los ribosomas en el citoplasma traducen dos secciones de ARN viral en largas cadenas de aminoácidos, que luego se dividen en 16 proteínas, incluidas muchas involucradas en la síntesis de ARN. Más tarde, se generan más ARNs que codifican para un total de 26 proteínas virales conocidas, incluidas las estructurales utilizadas para producir nuevas partículas de virus, como el pico, y otras proteínas accesorias. De esta manera, el virus comienza a producir copias de su propio ARN mensajero. Pero necesita la maquinaria de la célula para traducir esos ARNm en proteínas.
Relacionado: How a rampant coronavirus variant blunts our immune defences
Los coronavirus se apoderan de esa maquinaria de muchas maneras. La viróloga Noam Stern-Ginossar y su equipo en el Instituto Weizmann de Ciencias en Rehovot, Israel, se acercaron a tres mecanismos por los cuales el SARS-CoV-2 suprime la traducción del ARNm del huésped en favor de los suyos propios. Ninguno es exclusivo de este virus, pero la combinación, velocidad y magnitud de los efectos parecen únicos, dice Stern-Ginossar.
En primer lugar, el virus elimina la competencia: la proteína viral Nsp1, una de las primeras proteínas traducidas cuando llega el virus, recluta proteínas del huésped para cortar sistemáticamente todos los ARNm celulares que no tienen una etiqueta viral. Cuando el equipo de Stern-Ginossar puso esa misma etiqueta en el extremo de un ARNm huésped, el ARNm no se troceó [12].
En segundo lugar, la infección reduce la traducción general de proteínas en la célula en un 70%. Nsp1 es de nuevo el principal culpable, esta vez bloqueando físicamente el canal de entrada de los ribosomas para que el ARNm no pueda entrar, según el trabajo de dos equipos de investigación [13,14]. La poca capacidad de traducción que queda está dedicada a los ARNs virales, dice Stern-Ginossar.
Finalmente, el virus apaga el sistema de alarma de la célula. Esto sucede de muchas maneras, pero el equipo de Stern-Ginossar identificó un mecanismo claro para el SARS-CoV-2: el virus impide que el ARNm celular salga del núcleo, incluidas las instrucciones para las proteínas destinadas a alertar al sistema inmunológico de la infección. Un segundo equipo confirmó este hallazgo, y de nuevo señaló a Nsp1: la proteína parece atascar los canales de salida en el núcleo para que nada pueda escapar [15].
Debido a que las transcripciones de genes no pueden salir del núcleo, las células infectadas no liberan muchos interferones, estas son proteínas de señalización que alertan al sistema inmunitario sobre la presencia de un virus. El SARS-Cov-2 es particularmente eficiente para apagar este sistema de alarma: en comparación con otros virus respiratorios, como el SARS-CoV y el virus sincitial respiratorio, la infección por SARS-CoV-2 induce niveles significativamente más bajos de interferones [16]. Y este mes de junio, los investigadores reportaron mutaciones en la variante Alfa que parecen permitirle someter la producción de interferón de manera aún más eficiente [17].
«Está claro que el SARS-CoV-2 es un virus muy rápido que tiene una capacidad única para evitar que nuestro sistema inmunológico reconozca y comporte la infección en las primeras etapas», dice Stern-Ginossar. En el momento en que el sistema inmunológico se da cuenta de que hay un virus, hay tanto de él que las proteínas de respuesta inmune a veces inundan el torrente sanguíneo a un ritmo más rápido de lo normal, lo que puede causar daño. Los médicos vieron al principio de la pandemia que algunas personas con COVID-19 que se enferman gravemente se ven perjudicadas por una respuesta inmune hiperactiva al SARS-CoV-2, así como por el propio virus. Algunos tratamientos probados funcionan amortiguando esta respuesta inmunitaria.
Estación de renovación
Una vez que el virus se ha hecho cargo del aparato molecular de la traducción del huésped, comienza un cambio de imagen del hogar, remodelando ampliamente el interior y el exterior de la célula a sus necesidades.
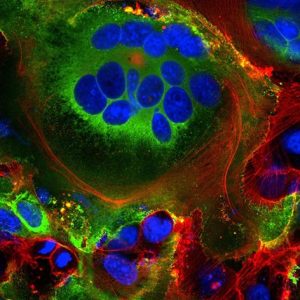
<– Fused cell structures (syncytia) seen in cells expressing the SARS-CoV-2 spike protein (green). Nuclei are in blue and the cell skeleton is in red.Credit: Mauro Giacca
En primer lugar, algunas de las proteínas espiga virales recién hechas viajan a la superficie de la célula y asoman fuera de la membrana de la célula huésped. Allí, activan un canal de iones de calcio del huésped, que expulsa una capa de grasa en el exterior de la célula, la misma capa que se encuentra en las células que se fusionan naturalmente, como las células musculares. En este punto, la célula infectada se fusiona con las células vecinas que expresan ACE2, desarrollándose en células respiratorias individuales masivas llenas de hasta 20 núcleos.
Fused cell structures (syncytia) seen in cells expressing the SARS-CoV-2 spike protein (green). Nuclei are in blue and the cell skeleton is in red.Credit: Mauro Giacca
Estas estructuras fusionadas, llamadas sinticios, son inducidas por infecciones virales como el VIH y el virus del herpes simple, pero no por el virus del SARS, dice el biólogo molecular Mauro Giacca del King’s College de Londres, quien dirigió el equipo que publicó el hallazgo en abril. Él presume que la formación de sinticios permite que las células infectadas prosperen durante largos períodos de tiempo, produciendo más y más viriones. «Este no es un virus de atropello y fuga», dice. «Persiste». Un segundo equipo, dirigido por el investigador Qiang Sun de la Academia China de Ciencias Médicas en Beijing, descubrió que algunas células infectadas por COVID-19 incluso forman sinticios con linfocitos —una de las propias células inmunitarias del cuerpo [19]—. Éste es un mecanismo sabido de la evasión inmune por las células del tumor, pero no por los virus. Sugiere que las células infectadas evitan la detección inmune simplemente agarrándose y fusionándose con los exploradores inmunes cercanos.
En el interior de la célula, se están produciendo aún más cambios. Al igual que otros coronavirus, el SARS-CoV-2 transforma el retículo endoplásmico largo y delgado (RE), una red de membranas planas involucradas en la síntesis y el transporte de proteínas, en esferas de doble membrana, como si el RE estuviera soplando burbujas. Estas vesículas de doble membrana (DMV) podrían proporcionar un lugar seguro para que el ARN viral se replique y traduzca, protegiándolo de los sensores inmunes innatos en la célula, pero esa hipótesis todavía se está investigando.
Las proteínas implicadas en la fabricación de DMV podrían ser buenas dianas farmacológicas, porque parecen ser necesarias para la replicación viral. Por ejemplo, se necesita una proteína huésped, TMEM41B, para movilizar el colesterol y otros lípidos para expandir las membranas del RE de modo que todas las partes del virus quepan dentro [20]. «Cuando sacas TMEM41B, tiene un gran impacto en la infección», dice Vineet Menachery, investigador de coronavirus en la Rama Médica de la Universidad de Texas en Galveston, quien participó en la investigación.
La proteína transmembrana del coronavirus Nsp3 también podría ser un objetivo: crea un poro en forma de corona en las paredes de los DMV para transportar el ARN viral recién hecho [21].
La mayoría de los virus que tienen un envoltorio externo, conocido como envoltura, forman esta característica por ensamblaje directamente en el borde de la célula, cooptando parte de la propia membrana plasmática de la célula en su salida. Pero las proteínas del coronavirus recién hechas toman un camino diferente.
Durante años, la evidencia ha sugerido que los coronavirus se transportan fuera de la célula a través del complejo de Golgi, un orgánulo que funciona como una oficina de correos, empaquetando moléculas en membranas y enviándolas a otras partes de la célula. Allí, el virus forma una envoltura lipídica de la membrana del complejo de Golgi; los viriones recién formados luego se llevan dentro de las vesículas de Golgi a la superficie celular, donde se escupen fuera de la célula, dice la viróloga y bióloga celular Carolyn Machamer de la Universidad Johns Hopkins en Baltimore, Maryland, quien ha estudiado los coronavirus durante 30 años.
Pero en diciembre, la bióloga celular Nihal Altan-Bonnet, del Instituto Nacional del Corazón, los Pulmones y la Sangre de Estados Unidos en Bethesda, Maryland, y sus colegas informaron que habían detectado coronavirus que salían de la célula a través de lisosomas, contenedores de basura celular llenos de enzimas que descomponen las partes celulares [22]. El bloqueo de la vía secretora basada en Golgi no parecía afectar la cantidad de virus infecciosos que se liberaban, dice Altan-Bonnet. La evidencia de su equipo sugiere que las proteínas virales forman una envoltura al brotar en la sala de emergencias, y luego se concentran en los lisosomas para salir de la célula. Los investigadores actualmente están probando inhibidores que bloquean el proceso de salida lisosomal como posibles candidatos antivirales.
Dejar una célula a través de los Golgi o lisosomas es lento e ineficiente en comparación con la brotación de una membrana plasmática, por lo que los científicos no saben por qué lo hace el SARS-CoV-2. Machamer sospecha que la composición lipídica de una envoltura derivada de Golgi o lisosoma es de alguna manera más beneficiosa para el virus que una de la membrana plasmática. «Si entendiéramos esta parte un poco mejor, habría grandes oportunidades para nuevas terapias antivirales», dice.
Última rebanada
En la salida de la célula, un evento más convierte a este virus en un gigante infeccioso: un rápido recorte en un sitio de cinco aminoácidos prepara al virus para alcanzar su próximo objetivo. Mientras que otros coronavirus tienen un solo aminoácido de arginina en la unión de las subunidades S1 y S2 de la espiga, el SARS-CoV-2 tiene una línea de cinco aminoácidos: prolina, arginina, arginina, alanina y arginina. «Debido a que el sitio era inusual, nos centramos en él, y resultó que, sí, el sitio es esencial para la invasión de las células pulmonares», dice Pöhlmann. En mayo de 2020, él y sus colegas informaron que una proteína de células huésped llamada furina reconoce y recorta esa cadena de aminoácidos, y el corte es «esencial» para que el virus entre de manera eficiente en las células pulmonares humanas [23].
No es la primera vez que los investigadores han identificado un sitio de escisión de furina en un virus; los virus de la influenza aviar altamente patógenos también lo tienen, dice Barclay. Cuando una colega envió a Barclay una cepa de SARS-CoV-2 en cultivo que había perdido espontáneamente el sitio de escisión de la furina, su equipo descubrió que los hurones infectados con esta cepa arrojaron partículas virales en cantidades menores que los infectados con la cepa pandémica, y no transmitieron la infección a los animales cercanos [9]. Al mismo tiempo que el equipo de Barclay informó de sus resultados en una preimpresión de septiembre de 2020, un estudio en los Países Bajos también encontró que el coronavirus con un sitio de escisión de furina intacto entra en las células de las vías respiratorias humanas más rápido que aquellos sin él [24].
Se sospecha que la Furina corta el sitio en algún momento durante el ensamblaje del virión, o justo antes de la liberación. El momento podría explicar por qué el virus sale a través de los Golgi o lisosomas, dice Tom Gallagher, virólogo de la Universidad Loyola de Chicago en Illinois. «El virus, una vez ensamblado, se mueve en un orgánulo donde se puede bañar en presencia de la proteasa de la furina».
Al cortar el enlace entre las subunidades S1 y S2, el corte de furina afloja las proteínas de espiga de virión para que durante la entrada celular respondan a un segundo corte por TMPRSS2, que expone el área hidrofóbica que se entierra rápidamente en una membrana de las células huésped, dice Gallagher. Si los picos no son pre-recortados por furina, y no siempre lo son, pasan por alto TMPRSS2, y entran a través de la vía endosomal más lenta, si es que lo hacen.
Relacionado: The race for antiviral drugs to beat COVID — and the next pandemic
Dos variantes del coronavirus, Alpha y Delta, han alterado los sitios de escisión de la furina. En la variante alfa, el aminoácido prolina inicial se cambia a una histidina (P681H); en la variante Delta, se cambia a una arginina (P681R). Ambos cambios hacen que la secuencia sea menos ácida, y cuanto más básica sea la cadena de aminoácidos, más eficazmente la furina la reconoce y la corta, dice Barclay. «Plantearíamos la hipótesis de que este es el virus que se está transmitiendo aún mejor».
Más cortes de furina significan más proteínas espiga preparadas para entrar en las células humanas. En el SARS-CoV, menos del 10% de las proteínas espigas están preparadas, dice Menachery, cuyo grupo de laboratorio ha estado cuantificando las proteínas espiga preparadas, pero aún no ha publicado este trabajo. En el SARS-CoV-2, ese porcentaje se eleva al 50%. En la variante Alfa, es más del 50%. En la variante delta altamente transmisible, el grupo ha encontrado, más del 75% de los picos están preparados para infectar una célula humana.
Incógnitas conocidas
La comunidad científica todavía está arañando la superficie de su comprensión del SARS-CoV-2. Las incógnitas clave incluyen el número de receptores ACE2 necesarios para unirse a cada proteína spike; cuando exactamente el sitio S2 es escindido por TMPRSS2; y el número de picos necesarios para la fusión virus-membrana celular, dice McLellan, y eso es solo para la entrada. En abril de 2020, un equipo de la Universidad de California en San Francisco identificó al menos 332 interacciones entre el SARS-CoV-2 y las proteínas humanas [25].
No es fácil seguir el ritmo del virus que muta rápidamente. La mayoría de las mutaciones hasta ahora están asociadas con la eficacia con la que se propaga el virus, no con cuánto daña el virus al huésped, coinciden los expertos. Este mes, un estudio informó que la variante Delta creció más rápidamente y en niveles más altos dentro de los pulmones y gargantas de las personas que las versiones anteriores del virus [26].
Pero aún no es seguro cómo las mutaciones de Delta han sobrealimentado la variante de esta manera, dice Stern-Ginossar. «Esto es algo que muchos laboratorios están tratando de averiguar».
Nature 595, 640-644 (2021)
doi: https://doi.org/10.1038/d41586-021-02039-y
References
[1] Casalino, L. et al. ACS Cent. Sci. 6, 1722–1734 (2020).
[2] Ke, Z. et al. Nature 588, 498–502 (2020).
[3] Turoňová, B. et al. Science 370, 203–208 (2020).
[4] Nguyen, H. L. et al. J. Phys. Chem. B 124, 7336–7347 (2020).
[5] Shang, J. et al. Nature 581, 221–224 (2020).
[6] Gobeil, S. M.-C. et al. Science https://doi.org/10.1126/science.abi6226 (2021).
[7] Khateeb, J., Li, Y. & Zhang, H. Crit. Care 25, 244 (2021).
[8} Hoffmann, M. et al. Cell 181, 271–280 (2020).
[9] Peacock, T. P. et al. Nature Microbiol. 6, 899–909 (2021).
[10] Wang, M. et al. Cell Res. 30, 269–271 (2020).
[11] Gunst, J. D. et al. EClinicalMedicine 35, 100894 (2021).
[12] Finkel, Y. et al. Nature 594, 240–245 (2021).
[13] Schubert, K. et al. Nature Struct. Mol. Biol. 27, 959–966 (2020).
[14] Thoms, M. et al. Science 369, 1249–1255 (2020).
[15] Zhang, K. et al. Sci. Adv. 7, eabe7386 (2021).
[16] Blanco-Melo, D. et al. Cell 181, 1036–1045 (2020).
[17Thorne, L. G. et al. Preprint at bioRxiv https://doi.org/10.1101/2021.06.06.446826 (2021).
[18] Braga, L. et al. Nature 594, 88–93 (2021).
[19]Zhang, Z. et al. Cell Death Differ. https://doi.org/10.1038/s41418-021-00782-3 (2021).
[20]Trimarco, J. D. et al. PLoS Pathog. 17, e1009599 (2021).
[21 Wolff, G. et al. Science 369, 1395–1398 (2020).
]PubMed Article Google Scholar
[22] Ghosh, S. et al. Cell 183, 1520–1535 (2020).
[23] Hoffmann, M., Kleine-Weber, H. & Pöhlmann, S. Mol. Cell 78, 779–784 (2020).
[24] Mykytyn, A. Z. et al. eLife 10, e64508 (2021).
[25] Gordon, D. E. et al. Nature 583, 459–468 (2020).
[26] Li, B. et al. Preprint at medRxiv https://doi.org/10.1101/2021.07.07.21260122 (2021).


