Resurgimiento de la infección por SARS-CoV-2 entre personal laboral del sistema de salud previamente vacunado.

Olvidos y edad.
01/09/2021
La sangría laboral de la Banca, permitida por políticos y sindicatos.
07/09/2021Por Jocelyn Keehner, M.D. y otros. Carta al editor de New England Journal of Medicine. Publicada el 1 de septiembre de 2021.
En diciembre de 2020, el personal laboral del University of California San Diego Health (UCSDH) experimentó un aumento dramático en las infecciones por coronavirus 2 (SARS-CoV-2) del síndrome respiratorio agudo severo. La vacunación con vacunas de ARNm comenzó a mediados de diciembre de 2020; en marzo, el 76% el personal laboral había sido completamente vacunado, y para julio, el porcentaje había aumentado al 83%. Las infecciones habían disminuido drásticamente a principios de febrero de 2021.
Entre marzo y junio, menos de 30 trabajadores de la salud dieron positivo cada mes. Sin embargo, coincidiendo con el final del mandato de llevar las mascarillas del 15 de junio en California y el rápido dominio de la variante B.1.617.2 (delta) que surgió por primera vez a mediados de abril y representó más del 95% de los aislamientos de UCSDH a fines de julio (Figura 1), las infecciones aumentaron rápidamente, incluidos los casos entre personas completamente vacunadas. Se obtuvo la aprobación de la junta de revisión institucional para el uso de datos administrativos sobre vacunas y datos de investigación de casos para examinar la efectividad de la vacuna contra el SARS CoV-2 del ARNm.
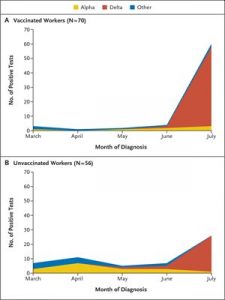
<– Figura 1. Variantes del SARS-CoV-2 entre trabajadores sanos sintomáticos.
El UCSDH tiene un umbral bajo para las pruebas de SARS-CoV-2, que se desencadena por la presencia de al menos un síntoma durante la detección diaria o por una exposición identificada, independientemente del estado de vacunación. Del 1 de marzo al 31 de julio de 2021, un total de 227 trabajadores de la salud del UCSDH dieron positivo para SARS-CoV-2 mediante el ensayo de reacción en cadena de la polimerasa cuantitativa con transcriptasa inversa (RT-qPCR) de hisopos nasales; 130 de los 227 trabajadores (57,3%) estaban completamente vacunados. Los síntomas estaban presentes en 109 de los 130 trabajadores completamente vacunados (83,8%) y en 80 de los 90 trabajadores no vacunados (88,9%). (Los 7 trabajadores restantes solo fueron vacunados parcialmente). No se notificaron muertes en ninguno de los grupos; una persona no vacunada fue hospitalizada por síntomas relacionados con el SARS-CoV-2.
Se calculó la efectividad de la vacuna para cada mes de marzo a julio; la definición de caso fue una prueba PCR positiva y uno o más síntomas entre personas sin infección previa por Covid-19 (ver el Apéndice Suplementario). La efectividad de la vacuna superó el 90% de marzo a junio, pero cayó al 65,5% (intervalo de confianza [IC] del 95%, 48,9 a 76,9) en julio (Tabla 1). Se analizaron las tasas de casos de julio según el mes en que los trabajadores con Covid-19 completaron la serie de vacunación; en los trabajadores que completaron la vacunación en enero o febrero, la tasa de ataque fue de 6,7 por 1000 personas (IC del 95%, 5,9 a 7,8), mientras que la tasa de ataque fue de 3,7 por 1000 personas (IC del 95%, 2,5 a 5,7) entre los que completaron la vacunación durante el período de marzo a mayo. Entre las personas no vacunadas, la tasa de ataques de julio fue de 16,4 por cada 1000 personas (IC del 95%, 11,8 a 22,9).
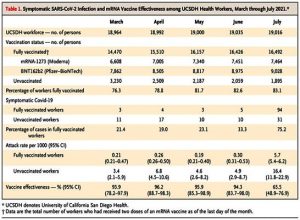
Tabla 1.- Infección sintomática por SARS-CoV-2 y efectividad de la vacuna de ARNm entre los trabajadores de salud de UCSDH, de marzo a julio de 2021. –>
Las vacunas de ARNm contra el SARS CoV-2, BNT162b2 (Pfizer-BioNTech) y ARNm-1273 (Moderna), han mostrado previamente tasas de eficacia del 95% y el 94,1%,2 respectivamente, en sus ensayos clínicos iniciales, y para la vacuna BNT162b2, mantuvieron, aunque ligeramente disminuida(84%) la eficacia 4 meses después de la segunda dosis. En Inglaterra, donde se utilizó un intervalo de dosificación extendido de hasta 12 semanas, López Bernal et al. reportaron una efectividad preservada de la vacuna del 88% contra la enfermedad sintomática asociada con la variante delta. Como observaron otros en poblaciones que recibieron vacunas de ARNm de acuerdo con los intervalos estándar de Autorización de Uso de Emergencia, nuestros datos sugieren que la efectividad de la vacuna contra cualquier enfermedad sintomática es considerablemente menor contra la variante delta y puede disminuir con el tiempo desde la vacunación.
Es probable que el cambio drástico en la efectividad de la vacuna de junio a julio se deba tanto a la aparición de la variante delta como a la disminución de la inmunidad con el tiempo, agravada por el fin de los requisitos de enmascaramiento en California y el mayor riesgo resultante de exposición en la comunidad. Nuestros hallazgos subrayan la importancia de restablecer rápidamente las intervenciones no farmacéuticas, como el enmascaramiento en interiores y las estrategias de pruebas intensivas, además de los esfuerzos continuos para aumentar las vacunas, como estrategias para prevenir enfermedades y muertes evitables y para evitar interrupciones masivas en la sociedad durante la propagación de esta formidable variante. Además, si nuestros hallazgos sobre la disminución de la inmunidad se verifican en otros entornos, pueden estar indicadas las dosis de refuerzo.
Jocelyn Keehner, M.D.
Lucy E. Horton, M.D., M.P.H.
UC San Diego Health, San Diego, CA
Nancy J. Binkin, M.D., M.P.H.
UC San Diego, La Jolla, CA
Louise C. Laurent, M.D., Ph.D.
David Pride, M.D., Ph.D.
Christopher A. Longhurst, M.D.
Shira R. Abeles, M.D.
Francesca J. Torriani, M.D.
UC San Diego Health, San Diego, CA
ftorriani@health.ucsd.edu
Disclosure forms provided by the authors are available with the full text of this letter at NEJM.org.
This letter was published on September 1, 2021, at NEJM.org.
Dr. Laurent serves as an author on behalf of the SEARCH Alliance. Collaborators in the SEARCH Alliance are listed in the Supplementary Appendix, available with the full text of this letter at NEJM.org.
Drs. Keehner and Horton and Drs. Abeles and Torriani contributed equally to this letter.