Investigación con quimeras humano-animales y modelos embrionarios. Valoración biomédica y ética.

Fetos de ratón, generados sin esperma ni óvulos por primera vez.
22/10/2019
25 años de la AEBI y 100 números de Cuadernos de Bioética.
28/10/2019 Por Justo Aznar, Lucía Gómez Tatay y Julio Tudela, Observatorio de Bioética. Instituto de Ciencias de la Vida. Universidad Católica de Valencia. Un “Informe sobre las últimas investigaciones del grupo de Juan Carlos izpisúa Belmonte. Valoración biomédica y ética”.
Por Justo Aznar, Lucía Gómez Tatay y Julio Tudela, Observatorio de Bioética. Instituto de Ciencias de la Vida. Universidad Católica de Valencia. Un “Informe sobre las últimas investigaciones del grupo de Juan Carlos izpisúa Belmonte. Valoración biomédica y ética”.
No cabe duda de la importancia que tienen investigaciones biomédicas del español Juan Carlos Izpisúa, ubicado principalmente en su laboratorio del Instituto Salk para Estudios Biológicos, en La  Jolla, California.
Jolla, California.
Los trabajos de Izpisúa se centran fundamentalmente en: la producción de híbridos o quimeras humano-animales; desarrollar métodos para hacer más eficiente la técnica CRISPR; y la reprogramación celular “in vivo “para prevenir el envejecimiento; pero ahora ha ampliado sus objetivos de investigación a la producción de embrioides humanos para ser utilizados en investigaciones biomédicas. Todos estos campos de investigación tienen una indudable importancia, tanto médica como social, pero también plantean objetivos problemas éticos.
Quimeras humano-animales
Sus experiencias para la creación de híbridos o quimeras se publicaron por primera vez en mayo de 2015, en un artículo en Nature. Esencialmente consistieron en inyectar células troncales embrionarias en embriones de ratones para que en ellos se pudieran generar órganos cuasi humanos, con la finalidad última de producir órganos con contenido celular humano, que pudieran ser utilizados para trasplantes en la clínica humana. Pero dada la dificultad que podría suponer el tamaño de dichos órganos, al realizarse las experiencias en ratones, en 2017 produjeron quimeras humano-animales con animales de mayor tamaño (cerdos y vacas).
Pero, no solamente el grupo de Izpisua, también otros grupos de investigación han dirigido sus trabajos a la producción de quimeras humano animales. Así, en un trabajo publicado el 25 de enero de 2017, en Nature, se describen las experiencias de un grupo de investigadores del Instituto de Biología de Células Madre y Medicina Regenerativa de la Universidad de Stanford, que han conseguido desarrollar un páncreas de ratón en ratas y, posteriormente, trasplantarlo con éxito desde las ratas a ratones con diabetes, en los que el órgano funcionó correctamente e hizo revertir la enfermedad. Para conseguirlo inyectaron células troncales pluripotentes de ratón en embriones de rata modificados genéticamente. La modificación consistió en la eliminación de un gen (Pdx1) necesario para la formación del páncreas. Al no poder las ratas producir su propio páncreas, las células de ratón lo produjeron. Estos resultados fueron prometedores, pues consiguieron revertir la diabetes en los ratones, normalizando sus niveles glucémicos durante 370 días. Además, solo se administraron inmunosupresores los cinco primeros días tras el injerto, no siendo necesarios posteriormente, pues el sistema inmunológico de los ratones eliminó las células residuales de rata, lo que podría suponer un gran paso adelante si estas experiencias pudieran trasladarse a la clínica humana.
No obstante, como señalan los propios autores, todavía falta mucho para poder aplicar esta tecnología en pacientes, cuyos órganos deberían formarse, por razones de tamaño y de distancia evolutiva, en cerdos, ovejas o primates no humanos.
 Como se ha comentado anteriormente, el 26 de enero de 2017, el grupo de Izpisúa publicó en Cell un nuevo trabajo en el que describían la producción de híbridos humano-cerdo y humano-vaca, pues aunque el ratón es uno de los modelos experimentales más útiles para la investigación con células troncales, sus diferencias con el ser humano son considerables, lo que puede obstaculizar no sólo la eficiencia, sino también la utilidad, de los estudios de quimeras humano-ratón. Es por ello por lo que Izpisúa y su equipo han utilizado cerdos y ganado vacuno para estudiar el potencial de las posibles quimeras utilizando diferentes tipos de células pluripotentes inducidas humanas (hiPSCs, por human induced pluripotent stem cells, en inglés). En dicho artículo, los investigadores reportan avances en múltiples frentes. En primer lugar, desarrollan páncreas, corazón y ojos de rata en embriones de ratón, combinando la tecnología de edición genética CRISPR-Cas9, con los últimos avances en células troncales. Como comenta J Wu, primer autor del trabajo, en un informe publicado en la página Web del Instituto Salk, sorprendentemente también se observó que las células pluripotentes de las ratas generaron una vesícula biliar en los ratones, un órgano que no está presente en las ratas, lo que llevo a afirmar que sus experimentos revelaban algo sorprendente, que un ratón en desarrollo es capaz de desbloquear el programa de formación de la vesícula biliar en las células de rata, en las que normalmente este programa se suprime durante su desarrollo. Esto destaca la importancia del nicho celular en el control del desarrollo organizacional y la especiación evolutiva.
Como se ha comentado anteriormente, el 26 de enero de 2017, el grupo de Izpisúa publicó en Cell un nuevo trabajo en el que describían la producción de híbridos humano-cerdo y humano-vaca, pues aunque el ratón es uno de los modelos experimentales más útiles para la investigación con células troncales, sus diferencias con el ser humano son considerables, lo que puede obstaculizar no sólo la eficiencia, sino también la utilidad, de los estudios de quimeras humano-ratón. Es por ello por lo que Izpisúa y su equipo han utilizado cerdos y ganado vacuno para estudiar el potencial de las posibles quimeras utilizando diferentes tipos de células pluripotentes inducidas humanas (hiPSCs, por human induced pluripotent stem cells, en inglés). En dicho artículo, los investigadores reportan avances en múltiples frentes. En primer lugar, desarrollan páncreas, corazón y ojos de rata en embriones de ratón, combinando la tecnología de edición genética CRISPR-Cas9, con los últimos avances en células troncales. Como comenta J Wu, primer autor del trabajo, en un informe publicado en la página Web del Instituto Salk, sorprendentemente también se observó que las células pluripotentes de las ratas generaron una vesícula biliar en los ratones, un órgano que no está presente en las ratas, lo que llevo a afirmar que sus experimentos revelaban algo sorprendente, que un ratón en desarrollo es capaz de desbloquear el programa de formación de la vesícula biliar en las células de rata, en las que normalmente este programa se suprime durante su desarrollo. Esto destaca la importancia del nicho celular en el control del desarrollo organizacional y la especiación evolutiva.
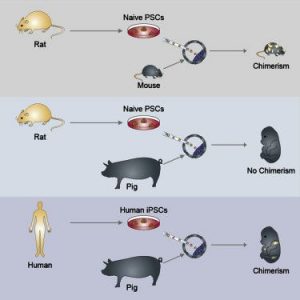 En un segundo experimento, generaron células y tejidos humanos en embriones preimplantados de cerdos y ganado, marcando el primer paso hacia la generación de órganos humanos trasplantables, al usar animales de mayor tamaño, cuya fisiología y anatomía son más similares a los humanos. Para ello, utilizaron diferentes tipos de células hiPS, que inyectaron a los embriones de cerdo y ganado vacuno, evaluando su capacidad de integración, para valorar su compatibilidad y potencial quimérico. Así, pudieron determinar los tipos celulares más prometedores. En una tercera y última fase, insertaron las células hiPS seleccionadas en embriones de cerdo, que posteriormente fueron gestados en cerdas adultas. En estas experiencias, los investigadores implantaron más de 2.000 embriones quiméricos en 41 cerdas, consiguiendo 18 embarazos. Tras la recolección embrionaria, entre los días 21-28 de desarrollo, se obtuvieron 186 embriones. Sin embargo, muchos de esos embriones eran de tamaño más pequeños de lo normal y crecieron mucho más lentamente.
En un segundo experimento, generaron células y tejidos humanos en embriones preimplantados de cerdos y ganado, marcando el primer paso hacia la generación de órganos humanos trasplantables, al usar animales de mayor tamaño, cuya fisiología y anatomía son más similares a los humanos. Para ello, utilizaron diferentes tipos de células hiPS, que inyectaron a los embriones de cerdo y ganado vacuno, evaluando su capacidad de integración, para valorar su compatibilidad y potencial quimérico. Así, pudieron determinar los tipos celulares más prometedores. En una tercera y última fase, insertaron las células hiPS seleccionadas en embriones de cerdo, que posteriormente fueron gestados en cerdas adultas. En estas experiencias, los investigadores implantaron más de 2.000 embriones quiméricos en 41 cerdas, consiguiendo 18 embarazos. Tras la recolección embrionaria, entre los días 21-28 de desarrollo, se obtuvieron 186 embriones. Sin embargo, muchos de esos embriones eran de tamaño más pequeños de lo normal y crecieron mucho más lentamente.
Ahora, el grupo de Izpizúa da un paso más en la producción de quimeras humano-animales, produciendo las primeras quimeras de humano y mono, en un laboratorio de China, según comenta a EL PAÍS su colaboradora Estrella Núñez, bióloga y Vicerrectora de investigación de la Universidad Católica de Murcia (UCAM)” [Fuente]. Los resultados aún no han sido publicados, pero en la noticia se indica que los monos quiméricos no llegaron a nacer, pues su gestación fue interrumpida.
Implicaciones bioéticas
La obtención de quimeras humano-animales, es decir, animales que albergan células humanas, y posiblemente en el futuro también tejidos y órganos, ofrece grandes posibilidades para investigaciones biomédicas, pero sobre todo para la producción de órganos para trasplantes.
Sin embargo, con independencia de su interés biomédico, estas experiencias plantean objetivos problemas bioéticos, que comentamos en un informe anterior, y que resumidamente podrían centrarse en que: a) en algunas de dichas experiencias se utilizaron células troncales de embriones humanos; b) no estaba totalmente controlado que las células humanas implantadas al animal no pudieran colonizar otros órganos distintos al que se pretende producir; c) que incluso dicha colonización podría alcanzar el cerebro humano o los órganos reproductores [Ver AQUI], lo que añadiría una dificultad bioética adicional; d) la amenaza de los límites conceptuales, sociales y morales que distinguen a los seres humanos de otras criaturas; y d) cuestiones de bioseguridad y bienestar animal.
Estas dificultades éticas también llevaron a que los Institutos Nacionales de Salud norteamericanos, anunciaran, en septiembre de 2015, que en adelante no financiarían investigaciones en las que se introdujeran células humanas pluripotentes en embriones de animales [Ver AQUI].
Estos problemas éticos han llevado a un consenso internacional que propugna interrumpir la gestación de los animales quiméricos a los 14 días, como se ha hecho ya en las experiencias aquí comentadas. Sin embargo, Japón se ha desvinculado de dicho consenso, al aprobar, en marzo de este año, nuevas normas que permiten la implantación de los embriones quiméricos en madres animales, así como su posterior nacimiento (ver AQUÍ).
Para tratar de obviar las dificultades éticas que estas técnicas presentan, los autores han propuesto utilizar un hecho biológico, que hace referencia a que, en el desarrollo embrionario de algunos órganos, como el páncreas y los riñones, éstos se generan por la acción de un solo gen, el Pdx1 y Six2, respectivamente. Así, sugieren que si se silencia el primero de estos genes se podrían producir cerdos sin páncreas, y si se silencia el segundo, cerdos sin riñones, lo cual podría tener una enorme importancia para sus investigaciones, pues las células troncales del otro organismo podrían colonizar el espacio dejado por el órgano ausente. Utilizando estas posibilidades, y la eliminación del único gen que se necesita para el desarrollo de un páncreas, el grupo de Izpisúa ha creado embriones de cerdos que no generan el órgano productor de insulina, a menos que se inyecten suficientes células troncales portadoras del gen que falta. Si las células añadidas se dividen de modo apropiado pueden dar lugar a un órgano maduro formado en su totalidad por células humanas. El resto del animal estará constituido, si todo se desarrolla normalmente, por células porcinas [ver AQUÍ]. Además, se podría eludir “el problema de la posible colonización por parte de células troncales humanas modificadas en tejidos no deseados, como el cerebro del animal, eliminando el programa genético que dirige el desarrollo neuronal de todas las células iPS antes de inyectarlas, de modo que, aunque dichas células lograsen migrar al nicho embrionario responsable del crecimiento del cerebro, no podrían seguir desarrollándose. Las únicas neuronas que lograrían hacerlo serían cien por cien porcinas” (Ver AQUÍ https://www.investigacionyciencia.es/revistas/investigacion-y-ciencia/la-gravedad-cuntica-a-prueba-693/rganos-humanos-fabricados-dentro-de-animales-14818).
Modelos embrionarios: embrioides
Siguiendo con sus investigaciones, ahora el equipo de Izpisúa, junto con investigadores de la Universidad de Texas, y del Instituto Salk, en California [ver AQUÍ], han publicado en la revista Cell la obtención in vitro de un “blastoide”, un modelo de embrión en estado de blastocisto, capaz de simular los primeros momentos del desarrollo embrionario in vitro e implantarse en el útero. En este trabajo cabe destacar que se ha conseguido obtener los blastoides a partir de células troncales derivadas de células adultas, por lo que prácticamente cualquier célula puede servir como base y no es necesario utilizar células procedentes de un embrión.
Este es un paso más en el campo de la investigación con embrioides o entidades sintéticas humanas con características embrionarias (SHEEFS, por sus siglas en inglés).En los últimos cinco años, el avance en la denominada “embriología sintética” se ha disparado, en concordancia con el auge del campo al que se adscribe esta ciencia, la investigación con organoides. Así, diversos estudios han demostrado que las células troncales de ratones y humanos pueden organizarse espontáneamente in vitro en estructuras 3D que son cada vez más similares a los embriones.
La utilidad de estos modelos radica en la posibilidad de emplearlos para el estudio del desarrollo embrionario, lo que puede arrojar luz sobre distintas complicaciones de la gestación o sobre el origen de determinadas enfermedades. Así mismo, Izpisúa destaca, en declaraciones a Diario Médico, que sus modelos embrionarios “catalizarán la investigación en muchas áreas diferentes para comprender los comienzos de la vida y promover la salud, para realizar pruebas de detección de tóxicos y drogas, para identificar factores ambientales perjudiciales” para el embrión, o, al contrario, sustancias que resulten útiles como “futuras terapias”.
Implicaciones bioéticas
Desde el punto de vista bioético, la posibilidad de obtener modelos in vitro para estudiar el desarrollo embrionario, sin tener que recurrir a un embrión humano real es sumamente atractiva. Sin embargo, es preocupante la posibilidad de que el perfeccionamiento de estos modelos pueda dar lugar a que en un futuro próximo se generen embriones humanos viables mediante dichas técnicas. En el trabajo que se comenta, algunos blastoides se implantaron en el útero de ratonas y generaron tejidos vivos, aunque desorganizados, no llegando a la producción de un embrión viable. No obstante, los propios autores señalan que su trabajo “allana el camino para producir embriones sintéticos viables mediante el uso de células cultivadas”, posibilidad que, de aplicarse en humanos, nos parece que sería éticamente inaceptable, pues cosificaría a esos embriones humanos producidos, conculcando su intrínseca dignidad.
Algunos dilemas bioéticos adicionales que estos experimentos plantean
La obtención de SHEEFS plantea los mismos dilemas éticos que suscita la obtención de clonotes o partenotes. Todos estos “embrioides” se asemejan, en una u otra medida, a los cigotos o blastocistos humanos obtenidos por fecundación de los gametos masculino y femenino, pero presentan diferencias genéticas en diferentes grados que impiden su división y crecimiento organizado hasta el estado fetal y posterior nacimiento. La magnitud de estas anomalías genéticas constituye el argumento que ha llevado a muchos científicos a considerarlos como no humanos.
En el caso de la clonación, las anomalías genéticas se producen por la inoculación del núcleo de una célula adulta en un ovocito enucleado, lo que implica que ha experimentado una evolución epigenética compleja, que lo diferencia del obtenido tras el sobrecruzamiento cromosómico que se produce tras la fecundación, en grado suficiente como para impedir su evolución hasta el nacimiento. Pero, en el caso de la clonación, estas diferencias ya han sido superadas en especies próximas a la humana, introduciendo modificaciones genéticas que han permitido recientemente el nacimiento de primates obtenidos por clonación.
En el caso de la partenogénesis, la obtención de “partenotes”, procedentes de ovocitos en los que se ha promovido la duplicación del material genético, convirtiéndolos en diploides y activándolos eléctricamente para promover su división, permite la obtención de embrioides con genomas de 46 cromosomas de procedencia humana, en este caso exclusivamente de ovocitos humanos, pero con las suficientes diferencias genéticas con respecto al cigoto obtenido por fecundación, como para no permitir su división más allá de un número limitado de células, lo que impide su progresión hasta el nacimiento. Pero, además, en este caso falta la aportación de la impronta genética masculina procedente del espermatozoide, imprescindible para la posterior evolución embrionaria. También, como en el caso anterior, no es descartable que la “reparación” genética de estas diferencias mediante las recientes herramientas de edición, permita en un futuro no lejano la obtención de fetos o el nacimiento de individuos procedentes de un partenote, que, en este caso, lo sería exclusivamente de mujeres.
En favor de estas técnicas se afirma que los embriones obtenidos, por no poder ser considerados embriones humanos, dadas las diferencias genéticas que poseen, podrían servir como fuente de células troncales, así como de material de investigación, cuya destrucción necesaria no implicaría los problemas bioéticos que se asocian a la destrucción de embriones humanos obtenidos por fecundación.
Entonces, ¿cuál es la dificultad bioética que implica la obtención de estos embrioides, incluidas las mencionadas SHEEFS? A nuestro juicio, radica en la imposibilidad de establecer límites claros en la magnitud de las diferencias genéticas con el embrión humano obtenido por fecundación, de modo que se pueda distinguir con claridad un embrión verdadero de un embrioide. Como es sabido, con determinada frecuencia los embriones humanos obtenidos por fecundación presentan errores genéticos en diverso grado que pueden, desde no afectar al fenotipo en absoluto, hasta hacerlos inviables, provocando su muerte en estadios muy tempranos de su vida embrionaria, sin que esto permita dejar de considerar humano a aquel cigoto o al embrión temprano que se deriva de él, aunque los defectos genéticos sobrevenidos lo hagan incompatible con su desarrollo normal. Entonces, ¿podría determinarse qué nivel preciso de alteración genética es necesario para considerar un cigoto o blastocisto como un ser humano o un mero agregado celular? ¿Diríamos que en los experimentos previos que llevaron a la obtención de cigotos clonados de macacos, que no eran capaces de dividirse hasta el nacimiento, no se trataba de verdaderos cigotos de macaco? ¿qué grado de reparación genética posible sería exigible para considerar que un embrioide pueda ser considerado embrión? La respuesta es incierta.
Conviene en este punto recordar que una sentencia del Tribunal de Justicia Europeo, dictada en Octubre de 2011 (Sentencia de 18.10.2011 – Asunto C-34/10, dictaminada explícitamente lo siguiente: “La sentencia confirma que la legislación europea relativa a la protección jurídica de las invenciones biotecnológicas debe interpretarse en el sentido de que constituye un “embrión humano” todo óvulo humano a partir del estadio de la fecundación, todo óvulo humano no fecundado en el que se haya implantado el núcleo de una célula humana madura, y todo óvulo humano no fecundado estimulado para dividirse y desarrollarse mediante partenogénesis”.
A la luz de este texto, parece que el principio de prudencia aconsejó, en este caso, la atribución del estatuto humano a los clonotes y partenotes, precisamente por la imposibilidad de establecer fronteras nítidas que permitan sistematizar el grado de las diferencias que deberían distinguir a los cigotos y embriones obtenidos por fecundación de los obtenidos por clonación, partenogénesis o desdiferenciación celular inducida, como el caso que nos ocupa.
Quizá este principio de prudencia bioética deba aplicarse a las actuales investigaciones con vistas a evitar que puedan atentar contra vidas humanas que, aún en estado muy imperfecto genéticamente, deban seguir considerándose como tales.


