Edición génica en embriones humanos. Consideraciones éticas

Charlie Gard se ha tenido que ir. ¿Por qué?
03/08/2017
Sentimiento y condena del atentado dé Barcelona
18/08/2017Por Nicolás Jouve. Catedrático Emérito de Genética.  Presidente de CiViCa.
Presidente de CiViCa.
El CRISPR-Cas9 es una tecnología desarrollada para editar, corregir secuencias de ADN, basado en un mecanismo natural que existe como un sistema inmune en las bacterias, descubierto hace unos veinte años por el investigador ilicitano Francis Mojica (ver al final artículos relacionados). Tras diversos avatares los investigadores han aprendido a utilizar en el laboratorio este sistema como una herramienta para hacer lo que se ha dado en llamar «la edición genómica» o “edición de genes”. Algo así como corregir las secuencias del ADN mediante la eliminación de bases nucleotídicas alteradas y su sustitución por bases correctas, que son las que poseen las versiones sanas de los mismos genes.
Debido a la simplicidad del sistema CRISPR-Cas9 para dirigir e inducir cortes en el ADN que se desea modificar, su uso se ha extendido rápidamente con múltiples aplicaciones en el mejoramiento de especies vegetales, animales y microorganismos y también para hacer “terapia génica” en el hombre, superando tecnologías más complejas y menos eficaces, que se habían desarrollado anteriormente para los mismos propósitos.
El caso es que este sistema permite aspirar a hacer terapia génica, es decir corregir genes implicados en enfermedades hereditarias con fines clínicos. A pesar de su reciente aparición, el CRISPR-Cas9 ya se ha empezado a aplicar mediante acciones en células somáticas de los pacientes que padecen enfermedades monogénicas. Por ejemplo está en ejecución un ensayo clínico de inmunoterapia muy prometedor para corregir las células del sistema inmunológico en pacientes de cáncer en quienes la quimioterapia y otros tratamientos convencionales han fallado. Del mismo modo, la idea es tratar de corregir el genoma para tratar enfermedades genéticas raras u otras no tan raras pero sí importantes, como la anemia falciforme, la fibrosis quística, la hemofilia B, la mucopolisacaridosis, la fibrosis quística, el corea de Huntington, etc. Todas estas enfermedades se caracterizan por tener en común una alteración conocida en el gen implicado y consistente en una modificación puntual de sus bases nucleotídicas, cuya sustitución por la secuencia de ADN correcta es abordable con cierta seguridad por el CRIPR-Cas9.
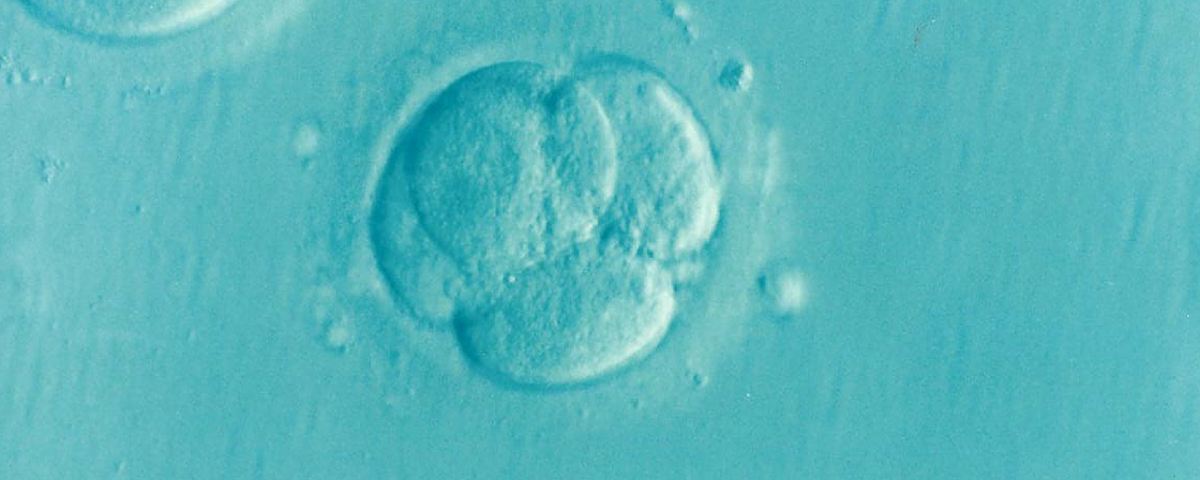
Acaba de publicarse el pasado 2 de Agosto en Nature (referencia al final) un artículo de investigadores de distintos países y en el que colabora también el investigador español Juan Carlos Izpisua Belmonte que va más allá de la corrección de patologías en células de pacientes adultos. Lo que se publica es la aplicación de las CRISPR-Cas9 para editar genes en embriones procedentes de la fecundación in vitro. Concretamente hacen experimentos de corrección de una mutación del gen MYBPC3, implicado en una cardiomiopatía, practicada en embriones humanos en fase muy inicial de desarrollo y procedentes de una pareja cuyo padre es portador de la alteración genética, heterocigosis. La madre no es portadora, por lo que la mitad de los embriones serían portadores heterocigóticos… y es en estos embriones donde se intenta la corrección del alelo alterado, lográndolo mediante la utilización del ADN del mismo gen no alterado, procdente de la madre para la reparación genética.
Hasta aquí todo parecería difícil pero caso de lograrlo muy prometedor para eliminar la región génica alterada. Lo que ocurre es que se hace en embriones que no han desarrollado aun la línea germinal… Si bien la corrección alcanzará a todas las células del individuo que se desarrolle a partir de estos embriones tras la implantación, hay varios problemas éticos.
En primer lugar la cantidad de embriones humanos que hay que producir y utilizar, muchos de los cuales se quedarán por el camino, ya que no hay un éxito 100%, ni en la corrección ni en la supervivencia. En segundo lugar, existe un gran problema de seguridad, por los posibles errores en la modificación de zonas del genoma que no se desean corregir (off target) pero para los que la CRISPR-Cas9 no garantiza su intervención. En otro trabajo, el Dr. Keith Joung del Massachusetts General Hospital y del laboratorio Harvard en Boston ha investigado sobre los lugares en que la enzima Cas9 puede actuar y ha detectado que provoca cortes en otros lugares del genoma, provocando alteraciones con frecuencias de mutación que van desde 0,1% a más del 60%, dependiendo de las células investigadas. Esto de ocurrir en embriones que no han desarrollado aun la línea germinal implica riesgos impredecibles de que la persona adulta que se desarrolle a partir de ellos transmita a sus descendientes alteraciones no detectadas pero potencialmente peligrosas para las futuras generaciones. Como casi todo lo que conlleva la manipulación genética, a pesar de la finalidad positiva de la técnica no se está libre de riesgos.
Sin embargo, ojala llegue el momento en que la tecnología CRISPR-Cas9 garantice la edición del gen sobre el que se desea incidir sin efectos sobre otras regiones del genoma… Mientras sería mejor no tocar los embriones y seguir investigando en células somáticas humanas cultivadas in vitro.
Referencia
Hong Ma et al. (2017) Correction of a pathogenic gene mutation in human embryos Nature, 2 August 2017, doi:10.1038/nature23305
Artículos previos sobre CRISPR-Cas9:
- Lo mejor en la investigación biomédica está por llegar – 26 de Marzo de 2015
- Hacia la nueva Humanidad -10 de Mayo de 2015
- La edición de genes con CRISPR ha salvado la vida de dos niños con leucemia27 de Enero de 2017
- La edición genética hoy. Su valoración bioética 20de Abril de 2017
- Edición génica en Tomate para corregir dos genes de interés25 de Mayo de2017
- El debate ético sobre la «edición» de genes humanos29 de Mayo de 2017