Un nuevo método de “edición genómica”, que incrementa la precisión.

Tarea del Observatorio One of Us para la dignidad de la persona. Por Elena Postigo Solana
22/10/2019
I Congreso Internacional sobre Naprotecnología, alternativa a la reproducción asistida.
22/10/2019 Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa.
Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa.
Hasta ahora la “edición genómica”, mediante la utilización de la técnica de CRISPR-Cas9, se había venido utilizando en su aplicación en Medicina fundamentalmente con fines clínicos, para tratar o prevenir una patología de causa genética en las células somáticas, no reproductivas, o para usos de investigación con el fin de conocer el funcionamiento de los genes en células de embriones o de la línea germinal [1,2]. A pesar de su mayor precisión y simplicidad que otras técnicas anteriores, los experimentos demostraban cierta inseguridad por la posibilidad de modificaciones fuera de destino (off-target), en otros lugares del genoma, o específicamente en aquellos que se deseaban corregir. Por ello, en diciembre de 2015, y más recientemente en Noviembre de 2018, las Academias Nacionales de Ciencias y Medicina de los Estados Unidos, entre otros entes, promovieron la celebración de Cumbres Internacionales sobre la Edición de Genes Humanos, en las que se ha reiterado la necesidad de establecer una moratoria voluntaria para la aplicación de estas nuevas tecnologías con fines de modificación del genoma de la línea germinal en los seres humanos, y la no utilización en embriones destinados a la implantación en el útero materno.
Un editorial de la revista Nature urgía sobre la importancia de crear un Observatorio Internacional Interdisciplinario e invitar a personas autorizadas cuyas voces e inquietudes son actualmente inaudibles para encauzar este tipo de investigaciones en centros de innovación biológica, y aprovechar así toda la riqueza de la imaginación moral de la humanidad [3].
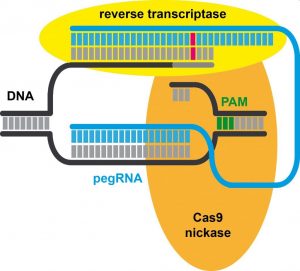 Un año después se produce una noticia importante con la aparición de una mejora sustancial de la técnica que aumenta considerablemente la precisión [4]. La mayoría de las variantes genéticas responsables de una enfermedad monogénica son difíciles de corregir de manera eficiente, precisamente por los posibles efectos sobre otras regiones del genoma. La nueva técnica, denominada de “edición primaria”, anunciada en Nature el 21 de octubre de 2019, consiste en un método de edición del genoma versátil y preciso que corrige directamente la información genética deseada, en un sitio específico del ADN. Para ello se utiliza una nueva enzima Cas9, con función de «nickasa» (productora de cortes en el ADN) y fusionada con una «transcriptasa inversa» de ingeniería, programada con un ARN guía para la transcripción primaria (pegRNA) que especifica el sitio de destino y codifica la edición deseada, todo de una vez.
Un año después se produce una noticia importante con la aparición de una mejora sustancial de la técnica que aumenta considerablemente la precisión [4]. La mayoría de las variantes genéticas responsables de una enfermedad monogénica son difíciles de corregir de manera eficiente, precisamente por los posibles efectos sobre otras regiones del genoma. La nueva técnica, denominada de “edición primaria”, anunciada en Nature el 21 de octubre de 2019, consiste en un método de edición del genoma versátil y preciso que corrige directamente la información genética deseada, en un sitio específico del ADN. Para ello se utiliza una nueva enzima Cas9, con función de «nickasa» (productora de cortes en el ADN) y fusionada con una «transcriptasa inversa» de ingeniería, programada con un ARN guía para la transcripción primaria (pegRNA) que especifica el sitio de destino y codifica la edición deseada, todo de una vez.
En el trabajo, dirigido por el Dr. David R. Liu (fotografía adjunta), del Howard Hughes Medical Institute de la Universidad de Harvard se realizaron más de 175 ediciones en células humanas, incluyendo inserciones dirigidas,  deleciones (pérdida de bases) y 12 tipos de mutación puntual sin necesidad de roturas de doble cadena o la adición de ADN molde corrector. Se aplicó la “edición primaria” en células humanas para corregir eficientemente y con pocos subproductos las secuencias de ADN implicadas en la anemia falciforme, en células falciformes (que requieren una edición en el gen HBB, el cambio de una base nucleotídica en el ADN del gen) y la enfermedad de Tay-Sachs (que requiere una deleción en el gen HEXA), con precisión en los lugares de destino. El desarrollo experimental se realizó en cuatro líneas celulares humanas y neuronas corticales de ratón con diferentes eficiencias.
deleciones (pérdida de bases) y 12 tipos de mutación puntual sin necesidad de roturas de doble cadena o la adición de ADN molde corrector. Se aplicó la “edición primaria” en células humanas para corregir eficientemente y con pocos subproductos las secuencias de ADN implicadas en la anemia falciforme, en células falciformes (que requieren una edición en el gen HBB, el cambio de una base nucleotídica en el ADN del gen) y la enfermedad de Tay-Sachs (que requiere una deleción en el gen HEXA), con precisión en los lugares de destino. El desarrollo experimental se realizó en cuatro líneas celulares humanas y neuronas corticales de ratón con diferentes eficiencias.
La “edición primaria” ofrece ventajas de eficiencia y pureza del producto sobre la reparación dirigida por homología, fortalezas y debilidades complementarias en comparación con la edición de bases, y una edición fuera de destino mucho menor que la nucleasa Cas9, hasta ahora utilizada en la tecnología CRISPR-Cas9. Según anuncia Nature, La nueva enzima amplía sustancialmente el alcance y las capacidades de la edición del genoma, y en principio podría corregir alrededor del 89% de las variantes genéticas humanas patógenas conocidas.
Si bien, con la nueva técnica aumenta la precisión y disminuyen los riesgos de un cambio incontrolado en otros lugares del genoma, habrá que seguir avanzando en la precisión antes que lanzarse a la aventura de su aplicación en cualquier tipo de células, y muy en particular en la linea germinal
[1] K. Niakan – K. Eggan, «Analysis of human embryos from zygote to blastocyst reveals distinct gene expression patterns relative to the mouse». Dev. Biol. 375 (2013) 54–64.
[2] H. Ma y otros, «Correction of a pathogenic gene mutation in human embryos». Nature 448 (2017) 413–419.
[3] Nature 555, 435, 2018.
[4] A.V. Anzalone, D.R. Liu y otros. «Search-and-replace genome editing without double-strand breaks or donor DNA». Nature, 26 October 2019. https://doi.org/10.1038/s41586-019-1711-4


