Las variantes del coronavirus no parecen ser altamente variables Hasta ahora SARS-CoV-2 puede estar estableciéndose en un conjunto limitado de mutaciones

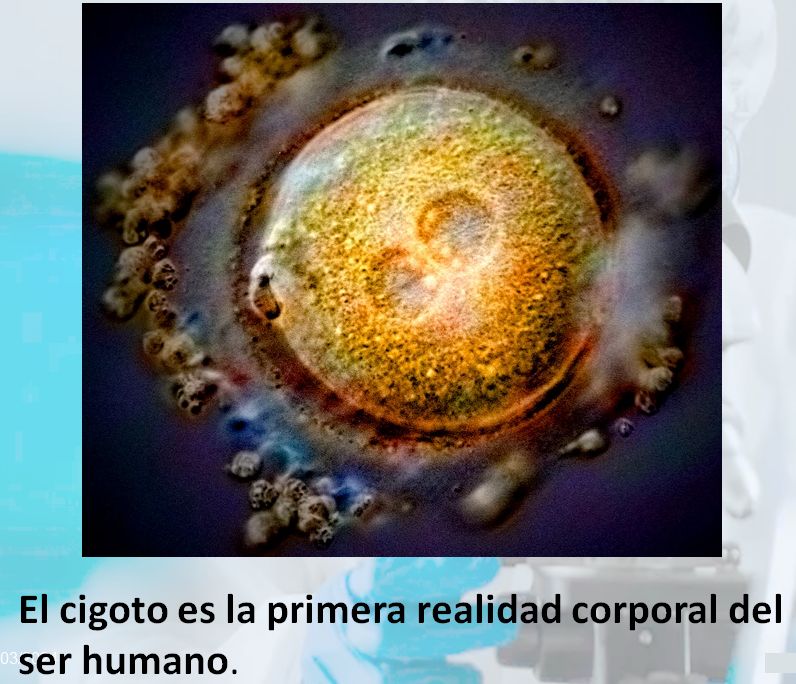
¿Es bioéticamente aceptable producir seudoembriones humanos para experimentaciones biológicas?
26/03/2021
Mons. Reig: «ESPAÑA TRANSFORMADA EN UN »CAMPO DE EXTERMINIO». Ante la aprobación de la ley de la Eutanasia»
31/03/2021Por Vaughn Cooper Ph.D., biólogo evolutivo y profesor de microbiología en la Universidad de Pittsburgh, Escuela de Medicina. Director del Centro de Biología Evolutiva y Medicina. Publicado en Scientific American el 24 de marzo de 2021 (Imagen de Portada: Jordan Siemens Getty Images)
Sin duda has oído hablar de las nuevas variantes de coronavirus que están evolucionando en todo el mundo. Ahora parece haber más de una docena de versiones de SARS-CoV-2, que son de diversos grados de preocupación porque algunas están vinculadas a una mayor infectividad y letalidad, mientras que otras no. Es fácil sentirse abrumado por esta diversidad y temer que nunca lograremos inmunidad de rebaño. Sin embargo, crece la evidencia de que estas variantes comparten combinaciones similares de mutaciones. Esta puede no ser la guerra multifronte que muchos temen, con un número infinito de nuevas versiones virales.
Soy un microbiólogo evolutivo que estudia cómo las bacterias y los virus se adaptan a nuevos entornos o huéspedes. Al igual que muchos microbiólogos, mis colegas y yo hemos centrado nuestra atención en entender cómo el SaRS-CoV-2 está evolucionando adaptaciones para reproducirse y transmitirse en humanos. Nuestro método de laboratorio favorito es la evolución experimental, donde cultivamos múltiples poblaciones de microbios a partir de la misma cepa en condiciones idénticas durante semanas o meses. Estudiamos problemas como cómo evoluciona la resistencia a los antibióticos y cómo las infecciones se vuelven crónicas. El poder de este método es que el uso de múltiples poblaciones nos permite «reproducir la cinta de la vida» y estudiar cuán repetible y, en última instancia, predecible podría ser la evolución.
Un patrón que vemos se llama evolución convergente, donde el mismo rasgo emerge en diferentes linajes independientes con el tiempo, generalmente a medida que se adaptan a entornos similares. Algunos de los mejores ejemplos de evolución convergente incluyen el color arenoso de diversos animales del desierto; aletas de natación lobuladas para ballenas, morsas y manatíes (que en realidad están distantemente relacionadas); e incluso la capacidad de los seres humanos para digerir la lactosa en la edad adulta, que surgió varias veces en poblaciones geográficamente aisladas.
En el caso del SARS-CoV-2, las secuencias completas del genoma de los virus de miles de pacientes nos permiten buscar patrones convergentes. Si bien la mayoría de las mutaciones son únicas y se extinguen, algunas establecen nuevos linajes que se vuelven más frecuentes a medida que el virus logra replicar e infectar a muchas personas. Si la misma parte del virus muta repetidamente en diferentes muestras en todo el mundo y se vuelve más frecuente, es muy probable que esta mutación codifique una adaptación que ayude al virus a reproducirse y transmitirse.
Con el beneficio de una mayor vigilancia del genoma del coronavirus, varios estudios recientes han identificado firmas de evolución convergente. Aquí en los Estados Unidos nuestro laboratorio encontró al menos siete linajes genéticamente independientes que adquirieron una mutación en un lugar en particular en la proteína de espiga del virus, la que utiliza para aferrarse a las células humanas. La proteína S tiene una secuencia de aminoácidos vinculados, y la mutación ocurre en la posición número 677. En el SARS-CoV-2 original este aminoácido es la glutamina, abreviadamente Q.
En seis linajes, Q ha mutado a otro aminoácido, la histidina (H) y se llama 677H. En el séptimo linaje, Q ha mutado a prolina (P). Cada linaje también tiene una mutación llamada S:614G, que fue el primer cambio notable en el virus que se identificó hace varios meses y se extendió tan ampliamente que ahora se encuentra en el 90 por ciento de todas las infecciones. Nombramos estos siete linajes estadounidenses en honor a las aves comunes —»robin», por ejemplo, y «pelícano»— para ayudarnos a distinguirlas y rastrearlas, y también para evitar crear prejuicios nombrándolas por primera vez en las áreas donde fueron detectadas por primera vez.
Los linajes fuera de los EE.UU. también han adquirido 677H, incluyendo las mutaciones de en Egipto, Dinamarca, India y un gran grupo en Macedonia. Una nueva variante de preocupación llamada B.1.525 también tiene 677H, al igual que varios linajes que descendieron de B.1.1.7, una de las primeras versiones preocupantes en ser detectadas. La aparición casual y global de mutaciones de S:677 y su quintuplicada ganancia en prevalencia ofrece una fuerte evidencia de que estos cambios deben mejorar la aptitud viral de alguna manera. Todavía no sabemos cómo, pero es notable que S:677 bordea una región de la proteína S que ayuda al virus a entrar e infectar las células humanas.
Esto está lejos del único ejemplo de convergencia en el SARS-CoV-2. Las mutaciones en al menos ocho posiciones diferentes en la proteína de la espícula están simultáneamente en aumento en todo el mundo, apareciendo en B.1.1.7 y en otras variantes importantes de preocupación conocidas como B.1.351, P.1 y P.3. Estas variantes comparten combinaciones de mutaciones en las posiciones 18, 69–70, 417, 452, 501, 681 y una mutación particularmente preocupante de E484K que evade anticuerpos neutralizantes. Por esta razón, dos de las principales webs científicos (http://covariants.org/ y http://outbreak.info) que rastrean variantes ahora informan de estas mutaciones compartidas y definitorias para simplificar y consolidar nuestra atención. El U.S. Centers for Disease Control y los medios de comunicación han tardado en seguir la importancia de estas mutaciones clave, pero esto está cambiando, porque son estos cambios los que probablemente alteran las funciones del virus como el contagio o la capacidad de evadir las vacunas.
Una forma de imaginar este tipo de evolución convergente es como un juego de Tetris, donde un número limitado de bloques de construcción se pueden ensamblar de diferentes maneras, en diferentes combinaciones, para lograr las mismas estructuras ganadoras. Por ejemplo, ahora se sabe que la combinación de mutaciones en B.1.1.7 lo hacen especialmente contagioso, y que el linaje B.1.351 puede evadir anticuerpos debido a E484K.
Debido a que muchas variantes recién descubiertas parecen estar remuestrenando las mutaciones encontradas en otras variantes establecidas, podemos especular que el virus está empezando a quedarse sin nuevas adaptaciones importantes. Pero esto no significa que las fuerzas de la evolución se detengan a medida que empecemos a acercarnos a la inmunidad de rebaño y relajar las restricciones. La historia nos dice que los virus pueden evolucionar rápidamente para evadir las barreras a la transmisión, especialmente cuando las infecciones siguen siendo numerosas. Debemos recordar que cuantas más infecciones haya, más posibilidades habrá de mutaciones, y proliferarán las que mejor ayuden al virus a sobrevivir. Esta es la razón por la que detener nuevas infecciones es clave. Estas adaptaciones virales ya están reescribiendo nuestros libros de texto de biología sobre la evolución convergente; vamos a esforzarnos por limitar el nuevo material.
También es fundamental que hagamos inversiones significativas en la construcción de un sistema de alerta temprana para detectar nuevas variantes SARS-CoV-2, así como muchos otros patógenos emergentes, tanto conocidos como aún por descubrir. La vigilancia y secuenciación del genoma viral es la clave. La razón por la que se han detectado muchas variantes en el Reino Unido se debe a las inversiones visionarias de investigadores y funcionarios de salud pública en estas tecnologías.
En los Estados Unidos, una afluencia significativa de dinero a los CDC del nuevo paquete de estímulo federal ya está aumentando la frecuencia con la que los investigadores pueden secuenciar y analizar muestras de virus. Esto debe mantenerse mediante la construcción de la experiencia en salud pública y la infraestructura de investigación para decodificar los cambios genéticos en el virus y anticipar la necesidad de futuras modificaciones de la vacuna. Fue la ciencia básica la que proporcionó esperanza en esta pandemia a través de la nueva tecnología de vacunas; y dado el renovado apoyo también será nuestro guardián contra futuras amenazas.