Las vacunas de ARNm y la candidatura al Nobel de Medicina.

XIII Congreso Internacional de la Asociación Española de Bioética y Ética Médica -AEBI
20/09/2021
España: Proposición de ley para penalizar a grupos provida.
22/09/2021 Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa y miembro del Comité de Bioética de España.
Por Nicolás Jouve, Catedrático Emérito de Genética, Presidente de CiViCa y miembro del Comité de Bioética de España.
Sin duda el éxito de la vacunación contra la COVID-19 es notable y en los medios sanitarios, científicos y académicos, aparte de los sociales, hay una gran coincidencia en señalar que el factor que ha frenado la pandemia ha sido la vacunación masiva iniciada a finales del año 2020.
De cualquier forma, debemos ser precavidos y continuar con las medidas mínimas de protección, pues aún sigue habiendo contagios, aunque sea en un grado mucho menor, al menos en España, al final de la llamada quinta ola. Lo que es evidente es que el bloqueo a la expansión es atribuible a las vacunas, como lo demuestra que en el momento presente los nuevos contagios se producen mayoritariamente en la población no vacunada, especialmente en los menores de 12 años…
Pero no olvidemos que, a su paso, la pandemia ha afectado a más de dos cientos millones y han fallecido cuatro millones y medio de personas en todo el mundo, además de las graves secuelas para la economía la vida laboral, cultural y social, y la merma de la libertad que ha supuesto este accidente de salud en todo el mundo, y muy especialmente en España.
Las vacunas deben llegar a todos
Además de la mayor o menor eficacia de unos sistemas de salud sorprendidos, y en muchos casos desbordados, por la rápida expansión del coronavirus, sin duda, el mérito de su bloqueo se debe a la rápida puesta a disposición de los servicios sanitarios de unas vacunas de calidad, eficaces y seguras, además de la logística de su distribución en todo el mundo, aunque, como siempre los últimos son probablemente los más necesitados. En este caso, los países pobres de los que no tenemos constancia ni datos fiables sobre cómo se está combatiendo la pandemia.
La desigual distribución de las vacunas hace que cuando quedan núcleos importantes de vacunación en muchas partes del mundo, existan otras en que parecen sobrar y hasta se pierden por rebasar la fecha de caducidad… Es importante poner solución a esto y atender cuanto antes a esas bolsas de la población más vulnerable, lo que redundará además en la reducción del problema a nivel mundial.
Recordemos lo que recomendaba la UNESCO en la Declaración en París sobre la COVID-19 del 6 de abril de 2020 cuando, entre otras advertencias, hacia un llamamiento a la cooperación y la solidaridad internacionales, en lugar de intereses nacionales de corto alcance, subrayando la responsabilidad de los países ricos de ayudar a las naciones pobres en este momento de emergencia de salud pública internacional.
Unas vacunas con un largo historial de investigación
Una de las coletillas más repetidos por quienes se oponen a las vacunas, en general, y a las que se desarrollaron en plena pandemia contra la COVID-19 desde principios de 2020, en particular, es que han sido improvisadas e inseguras por no contar con tiempo suficiente ni base científica para probar su seguridad y su eficacia. A este juicio se suele añadir que su comercialización ha sido improvisada y fruto de los intereses económicos de las empresas farmacéuticas que las han desarrollado.
Sin embargo, no debe olvidarse que la investigación en biotecnología al servicio de la salud es uno de los campos de mayor dinamismo e interés en el mundo y que nada era más importante que conseguir detener una pandemia que tanto dolor y tantas muertes estaba provocando desde su aparición en Wuhan a finales de 2019.
Ahora, que las vacunas han demostrado su validez y cuando la pandemia decae, es el momento de analizar las razones de su feliz obtención.
Entre las vacunas que más han contribuido al bloqueo de la pandemia destacan sin duda las llamadas “vacunas genéticas”, las de ARN mensajero. Se trata de las vacunas ‘Pfizer-NBiotech’ y ‘Moderna’, obtenidas tras unos ensayos clínicos acelerados por las circunstancias, pero con la suficiente garantía para aceptar su rápida aplicación. De hecho, ya en enero, se demostró su eficacia y seguridad en los primeros países en utilizarlas, Israel y el Reino Unido. Fueron las primeras en recibir la aprobación de la Organización Mundial de la Salud y la autorización de las Agencias nacionales e internaciones del Medicamento, tanto de la FDA (EE.UU.), como de la EMA (Agencia Europea del Medicamento).
A partir de su aprobación en diciembre de 2020, los países con mayores recursos empezaron a demandar estas vacunas, a las que se unirían después otras de tecnología más tradicional, al tiempo que crecía la impresión de su eficacia y su contribución a detener la pandemia. El objetivo era alcanzar cuanto antes la inmunidad de rebaño para bloquear la expansión del SARS-CoV2. Tal inmunidad se fijó en principio en un 70% de la población vacunada, si bien, por motivo de la aparición de cepas mutantes, la tasa de la población inmunizada se ha ido alargando hasta el 90%.
Pese a lo que se ha dicho, las vacunas no son fruto de la improvisación, sino de un largo historial de investigación, tanto básica como en su aplicación farmacológica. Las de ARN mensajero, si bien ha sido la primera vez que se han comercializado, tienen tras de sí décadas de investigación. Para su logro hay al menos tres avances que de forma complementaria han contribuido a su éxito:
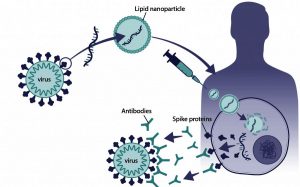
- Lo primero, y verosímilmente lo más importante, es la idea de introducir artificialmente moléculas de ARN mensajero en las células receptoras, con la información para la síntesis de proteínas capaces de generar una respuesta inmune. Es decir, utilizar el ARNm como un fármaco.
- Lo segundo, no menos importante, perfeccionar las condiciones que habría de tener la molécula sintética del ARNm para lograr su correcta expresión en el interior de las células receptoras.
- Lo tercero, habilitar un método para facilitar la entrada de las moléculas de ARNm de forma eficaz en las células receptoras. Para ello se han ensayado diversos sistemas utilizando gotitas de grasa.
 Cada una de estas aportaciones tiene sus propias vías de investigación, diferentes investigadores, laboratorios y proyectos, que han contribuido de forma integral al éxito final. Hay además una pléyade de compañías farmacéuticas y biotecnológicas que, han creído en estas investigaciones y han apostado por ellas, favoreciendo y creando los productos que al final han llegado a la población.
Cada una de estas aportaciones tiene sus propias vías de investigación, diferentes investigadores, laboratorios y proyectos, que han contribuido de forma integral al éxito final. Hay además una pléyade de compañías farmacéuticas y biotecnológicas que, han creído en estas investigaciones y han apostado por ellas, favoreciendo y creando los productos que al final han llegado a la población.
Respecto al primer avance importante, la idea de utilizar el ARNm como fármaco, todo empezó cuando a finales de 1987, Robert Malone, un estudiante estadounidense graduado en el Instituto Salk de Estudios Biológicos en La Jolla, California, realizó un experimento histórico. Mezcló cadenas de ARN mensajero con gotitas de grasa, para crear un preparado molecular. Las células humanas bañadas en este preparado genético absorbían el ARNm y lo traducían, produciendo las proteínas correspondientes a su mensaje genético [1]. Malone dejó escritas unas notas sobre este hallazgo el 11 de enero de 1988. Sin duda, esta investigación fue el primer peldaño, la piedra angular para la obtención de las vacunas de ARNm. Sin embargo, las dificultades técnicas y económicas determinaron que se abandonara temporalmente el camino iniciado por Malone.
La idea fue reactivada por el microbiólogo estadounidense Eli Gilboa, de la Universidad de Miami, que, en 1997, llevó a cabo la fundación de la primera compañía terapéutica de ARNm con el fin de combatir el cáncer. Se interesó por el desarrollo de vacunas personalizadas de células dendríticas con antígenos codificados en el ARNm para combatir tumores. Sus primeros resultados tuvieron lugar en el Centro Médico de la Universidad de Duke en Durham, Carolina del Norte [2]. Este trabajo indujo a los fundadores de las firmas alemanas CureVac y BioNTech, dos de las compañías de ARNm más grandes que existen en la actualidad, a comenzar a trabajar en ARNm.
El segundo paso, importante surgió cuando se atacaron las condiciones que debe tener el ARNm sintetizado en el laboratorio para su correcta expresión en las células receptoras. La bioquímica húngara Katalin Karikó y el inmunólogo estadounidense Drew Weissman, entonces en la Universidad de Pensilvania (UPenn) en Filadelfia, hicieron lo que ahora se reconoce como un hallazgo clave para el logro de las vacunas de ARNm. La alteración de algunas de las bases nucleotídicas del ARNm para facilitar su dispensación y conseguir que resista las defensas inmunes innatas de las células receptoras. En 2005, estos investigadores informaron que sustituir uno de los nucleótidos del ARNm, la uridina, por un análogo llamado pseudouridina, impedía que el cuerpo identificara el ARNm como un enemigo [3].
A ello se unió, el biólogo Derrick Rossi, que trabajaba en células madre en el Boston Children’s Hospital en Massachusetts y a la postre fundaría de la empresa farmacéutica Moderna. Rossi demostró que los ARNm modificados podrían usarse para transformar las células de la piel, primero en células madre embrionarias y luego en tejido muscular en contracción [4].
La tercera pieza clave para la obtención de estas vacunas, sería la de conseguir un modo eficaz de introducción del ARNm en las células humanas. Se debe al bioquímico y biólogo molecular canadiense Pieter Cullis, de la Universidad de Columbia Británica en Vancouver, que ya desde 1990 venía trabajando en una innovación crucial. Se trata de unas pequeñas burbujas de grasa conocidas como nanopartículas lipídicas, o LNPs, que protegen el ARNm y lo transportan a las células. Las vacunas de Pfizer-BioNTech, Moderna y CureVac, utilizan diversas combinaciones de estos compuestos. Sin duda, la entrada del ARNm en nuestras células no habría sido posible sin el trabajo de Pieter Cullis.
Los futuros Nobel de Medicina
 Lo que parece unánime en la opinión del mundo de las investigaciones biomédicas es que el próximo premio Nobel de Medicina le será otorgado a los investigadores que han contribuido a la producción de las vacunas de ARNm contra la COVID-19, sin olvidar los otros modos de obtención que, aunque menos innovadoras, han contribuido al bloqueo de la pandemia en todo el mundo. El problema surge al constatar la gran cantidad de investigadores que han contribuido a este gran logro, y la calidad de sus trabajos que conjuntamente lo han permitido.
Lo que parece unánime en la opinión del mundo de las investigaciones biomédicas es que el próximo premio Nobel de Medicina le será otorgado a los investigadores que han contribuido a la producción de las vacunas de ARNm contra la COVID-19, sin olvidar los otros modos de obtención que, aunque menos innovadoras, han contribuido al bloqueo de la pandemia en todo el mundo. El problema surge al constatar la gran cantidad de investigadores que han contribuido a este gran logro, y la calidad de sus trabajos que conjuntamente lo han permitido.
En cualquier caso, si como era costumbre. el premio Nobel de cualquier campo se adjudicaba al promotor de la idea que da lugar al avance científico objeto del premio, habrá que considerar en primer lugar al biólogo molecular y virólogo Robert Malone. Hay que decir “era”, y no “es”, costumbre, por lo que ocurrió el año pasado con el Nobel de Química, otorgado con toda justicia a la francesa Emmanuelle Carpentier y la americana Jennifer Doubna, por la propuesta de aplicación de la revolucionaria tecnología del CRISPR-Cas para la edición de genes con fines clínicos, pero con el imperdonable olvido del español Francisco Mojica, auténtico descubridor del sistema CRISPR-Cas que haría posible tal aplicación. Si nos ceñimos a la idea original, como ha sido tradición en la adjudicación de los premios Nobel, el primer candidato debe ser Robert Malone, pionero en la introducción del ARNm como fármaco, ya a finales de los años ochenta.
Pero, además, este año el Nobel de Medicina cuenta con muchos candidatos y variadas e importantes razones para su adjudicación. De hecho, el pasado 14 de septiembre la revista Nature publicaba un extenso artículo titulado La enmarañada historia de las vacunas de ARNm, en el que explicaba paso a paso y con todo detalle cómo se gestaron estas vacunas, que como hemos visto tienen tras de sí una historia de décadas de trabajo y decenas de investigadores implicados. Además, en el artículo se describen las decenas de empresas, spin-off, farmacéuticas y laboratorios que han intervenido, las disputas y los problemas de patentes y económicos por el enorme coste de los proyectos, muchas veces de dudoso éxito.
Si finalmente el Premio Nobel de Medicina recae en los creadores de la tecnología del ARNm, hay decenas de candidatos que han intervenido con mayor o menor mérito. Pero si nos ceñimos a las tres ideas o pasos fundamentales indicados anteriormente, la lista se reduce a unos pocos muy señalados.
Además de Robert Malone, entre quienes aparecen como candidatos principales estarían la bioquímica húngara Katalin Karikó y el inmunólogo estadounidense Drew Weissman, ya ganadores del Premio Princesa de Asturias de España a la Investigación Técnica y Científica 2021 (compartido con el inmunólogo estadounidense Philip Felgner, el médico turco Uğur Şahin, el médico alemán Özlem Türeci, el biólogo canadiense Derrick Rossi y la microbióloga inglesa Sarah Gilbert, todos ellos protagonistas de importantes de diferentes aspectos de la vacunación contra la Covid-19).
Finalmente, en la lista de los candidatos principales debería figurar el bioquímico canadiense Pieter Cullis, a quien se debe la importante consecución de un sistema eficaz de dispensación del ARNm en las células humanas.
Pronto sabremos a quien se le otorgan los premios Nobel de Medicina de este año. Pero por encima de todo está el hecho de la importancia de la investigación, tanto básica como aplicada para contribuir al bienestar de la humanidad. Sea el que sea el plantel de los premiados se merecen un agradecimiento muy especial por su contribución a una de las páginas más brillantes de la historia de la ciencia y de la medicina en los últimos decenios.
Referencias
[1] Malone, R. W., Felgner, P. L. & Verma, I. M. Proc. Natl Acad. Sci. USA 86, 6077–6081 (1989).
[2] Boczkowski, D., Nair, S. K., Snyder, D. & Gilboa, E. J. Exp. Med. 184, 465–472 (1996).
[3] Karikó, K., Buckstein, M., Ni, H. & Weissman, D. Immunity 23, 165–175 (2005).
[4] Warren, L. et al. Cell Stem Cell 7, 618–630 (2010).